

| A. | 氧化汞$\stackrel{加热}{→}$氧气+金属汞 | B. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 水$\stackrel{通电}{→}$氢气+氧气 | D. | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 |
分析 阴影部分既是化合反应又是氧化反应,化合反应是指由两种或两种以上物质反应生成另外一种物质的反应,其特征是“多变一”;物质与氧发生的化学反应属于氧化反应,进行分析判断.
解答 解:阴影部分既是化合反应又是氧化反应.
A、氧化汞$\stackrel{加热}{→}$氧气+金属汞,该反应符合“一变多”的特征,属于分解反应,故选项错误.
B、酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水,该反应的生成物是两种,不符合“多变一”的特征,不属于化合反应,故选项错误.
C、水$\stackrel{通电}{→}$氢气+氧气,该反应符合“一变多”的特征,属于分解反应,故选项错误.
D、硫+氧气$\stackrel{点燃}{→}$二氧化硫,该反应符合“多变一”的特征,属于化合反应;又是物质与氧气发生的反应,属于氧化反应;故选项正确.
故选:D.
点评 本题难度不大,掌握化合反应的特征(“多变一”)、氧化反应的特征并能灵活运用是正确解答本题的关键.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 重氢原子核外有两个电子 | |
| B. | 重水分子由普通氢原子、氧原子构成 | |
| C. | 重氢离子核内有一个质子 | |
| D. | 氢原子和重氢原子化学性质不一样 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 硝酸钾 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
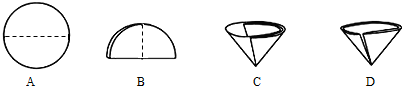
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有(1)、(2)组溶液呈蓝色,且一定有沉淀出现 | |
| B. | 只有(1)组液体中,一定有不溶物生成 | |
| C. | 只有(2)、(4)组液体中,不可能出现浑浊 | |
| D. | 四组液体中一定都会出现沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
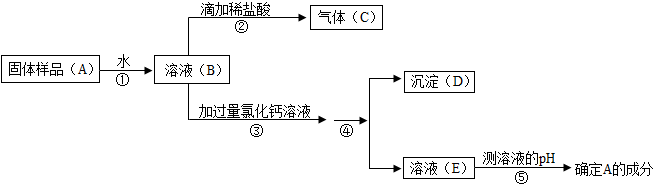
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
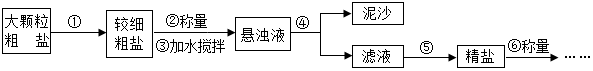
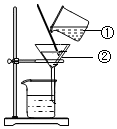 如图所示为粗盐精制的示意图,回答:
如图所示为粗盐精制的示意图,回答:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
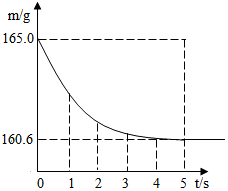 在烧杯中加入氯化钠和碳酸氢钠的固体混合物10g后,再加入68.9g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g,已知反应的化学方程式为:NaHCO3+HCl═NaCl+CO2↑+H2O.试回答下列问题:
在烧杯中加入氯化钠和碳酸氢钠的固体混合物10g后,再加入68.9g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g,已知反应的化学方程式为:NaHCO3+HCl═NaCl+CO2↑+H2O.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于氧化物 | |
| B. | 柠檬酸中碳、氢、氧三种元素的质量比为9:1:14 | |
| C. | 19.2g柠檬酸中碳元素的质量是1.2g | |
| D. | 柠檬酸中所含氢元素的质量分数为$\frac{8}{12+8+16}$×100% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com