
某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把100g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,也不与稀盐酸反应)。请计算:
序号 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
第一次 | 25 | 13 |
第二次 | 25 | 6 |
第三次 | 25 | 2 |
第四次 | 25 | n |
(1)表中n的数值为_____________。
(2)求反应生成的二氧化碳的质量是多少_______?(写出计算过程)
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源:江苏省盐城市盐都区2019届九年级第一学期期末质量检测化学试卷 题型:单选题
下列实验方案不能够达到相应实验目的的是
实验目的 | 实验方案 | |
A | 比较 Fe、Cu、Ag 的金属活动性 | 将铁丝分别浸入 CuSO4 溶液和 AgNO3 溶液 |
B | 用最好的方法把室温下的不饱和食盐水变成饱和溶液 | 加食盐 |
C | 除去二氧化锰固体中混有的少量氯化钾 | 加水溶解、过滤、洗涤、干燥 |
D | 区分黄金和黄铜片 | 灼烧 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源:内蒙古乌海市2019届九年级上学期期末考试化学试卷 题型:单选题
实验证明M气体在空气中燃烧有CO2生成.仅根据此结果,对M的成分推测正确的是( )
A. M是一氧化碳
B. M是甲烷
C. M中一定含有碳元素
D. M中含有碳、氧两种元素
查看答案和解析>>
科目:初中化学 来源:福建省泉州市2019届九年级上学期期末考试化学试卷 题型:填空题
阅读材料并回答相关问题
钴(Co)是一种银白色的金属、硬度大。常温下,钴在潮湿的空气中不会被锈蚀;加热时,钴会与氯气、硫等起化学作用,生成氯化物、硫化物等,其中二氯化钴(CoCl2)吸水后由蓝色变成了红色。 在工业上,钴可以制成多种合金;在医疗上,钴的一种化合物是维生素B12的主要成分,可用来医治恶性贫血、气喘、脊髓肋病等。
(1)写出金属钴的一条物理性质:______。
(2)已知二氯化钴和硫化钴中钴元素的化合价相同,请写出硫化钴的化学式______。
(3)图1为钴原子结构示意图,图2为钴元素在元素周期表中的部分信息。

①钴原子在化学反应中容易______(填“得到”或“失去”)电子。
②请把图2的信息补充完整。______
(4)下列说法不正确的是______(填标号)。
A.钴合金的硬度大于钴
B.钴及其化合物均无需密封保存
C.人体缺乏钴元素可以补充维生素B12
D.二氯化钴可用于检验物质是否含有水
查看答案和解析>>
科目:初中化学 来源:福建省泉州市2019届九年级上学期期末考试化学试卷 题型:单选题
亮氨酸(C6H13NO2)是人体必需的氨基酸之一,下列有关亮氨酸的说法错误的是
A. 由4种元素组成 B. 碳元素的质量分数最大 C. 含有氧分子 D. 碳、氧元素的质量比为9︰4
查看答案和解析>>
科目:初中化学 来源:江苏省等三校2019届九年级上学期期末联考化学试卷 题型:填空题
联系已学的化学知识,回答下列问题
(1)属于大气污染物的是_______(填“CO2”或“CO”);
(2)地壳中含量最多的金属元素是_________(填“铁”或“铝”);
(3)能形成酸雨的是______(填“CO2”或“SO2”);
(4)冶炼铁是利用CO的______(填“还原性”或“可燃性”);
查看答案和解析>>
科目:初中化学 来源:江苏省等三校2019届九年级上学期期末联考化学试卷 题型:单选题
逻辑推理是化学学习中常用的思维方法,下列推理正确的是
A. 碱的水溶液通常呈碱性,所以呈碱性的溶液一定是碱溶液
B. 化合物由不同种元素组成,所以由不同元素组成的纯净物一定是化合物
C. 化学变化伴随着能量的变化,则有能量变化的一定是化学变化
D. 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
查看答案和解析>>
科目:初中化学 来源:江西省于都县2019届九年级上学期期末考试化学试卷 题型:选择填充题
在我们的生活中发生着许多的变化,其中属于化学变化的是:(_______)
A.糯米酿酒 B.水的蒸馏 C.干冰升华 D. __________
查看答案和解析>>
科目:初中化学 来源:贵州省遵义市2019届九年级上学期期末测试化学试卷 题型:综合题
人类的生活、生产离不开金属。大自然向人类提供了丰富的金属矿物资源,人类每年提取量较大的金属是铁、铝、铜。
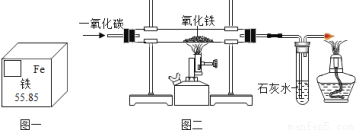
(1)根据铁在元素周期表中的信息(如图一),下列说法正确的是____。
A.方框内的数值即核内中子数为 26
B.铁的相对原子质量为 55.85g
C.铁元素在化学反应中易失去电子
D.铁离子的符号为 Fe2+
(2)防止铁制品锈蚀的措施有______(填一条)
(3)如图二所示是实验室用 CO 还原氧化铁的反应,玻璃管内的现象是_____,右端酒精灯的作用的是____。
(4)请你设计简单的实验,证明锌、铁、铜的活动性顺序,写出实验步骤、现象和结论。
实验步骤 | 实验现象 | 实现结论 |
________ | _______ | _______ |
(5)黄铜是铜锌合金,为测定某黄铜样品中铜的含量,取该黄铜样品 10g,放入足量稀盐酸中充分反应后,收集到 0.2g 氢气,请计算黄铜样品中铜的质量分数_______。(写出解题步骤)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com