
【题目】下图是元素周期表的一部分,请根据表中提供的信息按要求填空:
3Li | 4Be | 5B | ① | 7N | ② | 9F | 10Ne |
③ | 12Mg | ④ | 14Si | ⑤ | 16S | 17Cl | 18Ar |
(1)由⑤元素组成的单质在空气中燃烧的化学方程式为 。
(2)由①②③三种元素组成的物质为 。
(3)在元素周期表中,同一行元素最外层电子数的变化规律是 。
【答案】(1)4P+5O2![]() =2P2O5
=2P2O5
(2)Na2CO3
(3)由1至8逐渐增大
【解析】
(1)由表中提供的信息可知,原子序数:16>⑤>14,故⑤为15号元素磷,故可推测其燃烧的化学方程式;
(2)由表中提供的信息可知,①②③分别为碳元素、氧元素、钠元素,故可知其组成的常用物质名称;
(3)总结归纳在元素周期表中,同一行元素最外层电子数的变化规律.
解:(1)由表中提供的信息可知,原子序数:16>⑤>14,故⑤为15号元素磷,故可推测其燃烧的化学方程式为:4P+5O2![]() 2P2O5
2P2O5
(2)由表中提供的信息可知,①②③分别为碳元素、氧元素、钠元素,故可知其组成的常用物质名称为碳酸钠,其化学式为:已知钠元素的化合价为+1价,碳酸根的化合价为-2价,标注化合价![]() ,利用化合价数值交叉法书写化学式Na2CO3;
,利用化合价数值交叉法书写化学式Na2CO3;
(3)总结归纳在元素周期表中,同一行元素最外层电子数的变化规律由1至8逐渐增大.
故答为:(1)4P+5O2![]() 2P2O5
2P2O5
(2)Na2CO3;
(3)由1至8逐渐增大.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:
【题目】某同学为验证炭在氧气中不完全燃烧的产物既有CO又有CO2,设计如图所示流程进行实验,根据所学知识回答相关问题.(C装置中浓硫酸起干燥气体的作用)
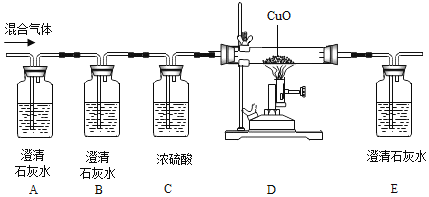
(1)按上面连接好装置,在装入药品之前,必须进行的操作是__________;
(2)A装置中澄清石灰水的作用是_______________;
(3)开始时,须先通入混合气体一段时间再点燃酒精喷灯加热,目的是_______;
(4)根据设计意图,观察到___________(填写实验现象)时,证明混合气体中既有CO又有CO2;
(5)从环保角度分析,该流程设计中的一处明显不足是____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种物质的溶解度曲线,请回答:
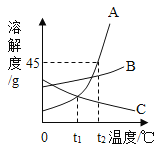
(1)在t2℃时,A、B、C三种物质的饱和溶液中溶质的质量分数由大到小的顺序为_____。
(2)将t2℃三种物质的饱和溶液降温至t1℃时溶质的质量分数由大到小的顺序是_____。
(3)要使接近饱和的C溶液变成饱和溶液,可采用的方法有_____(写出一种)。
(4)t2℃时,将30g A放入50g水中,所得溶液溶质的质量分数为_____(精确至0.1%)。
(5)写出一组符合图中趋势的三种物质的化学式,A_____,B_____,C_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A~E是初中化学常见的物质,且都含有一种相同的元素,A、C、D所属物质类别相同:“A-B”的反应可用于工业除铁锈;它们相互间的关系如下图所示。
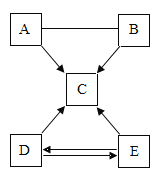
(“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系)
(1)若E为单质,通过动植物呼吸作用可实现E→D的转化,则E的化学式是________;通过绿色植物的________作用,可实现D→E的转化。
(2)写出A与B反应的化学方程式________。
(3)者B和E属于同一类物质,则C的化学式是:________。在转化为C的四个反应中,不涉及到的基本反应类型是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
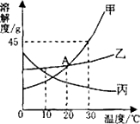
(1)A点的含义是_____________________。
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液是____________溶液(填“饱和”或“不饱和”)。
(3)若乙中混有少量甲,最好采用_________的方法提纯乙(填“降温结晶”或“蒸发结晶”)。
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应都遵守质量守恒定律,请根据质量守恒定律的相关知识完成下列
(1)下列各项中,在化学反应前后一定不变的是________ (填数字序号).
①元素的种类 ②物质的种类③原子的种类 ④分子的种类⑤原子的数目⑥分子的数目
(2)应用质量守恒定律配平化学方程式:____FeS2+ ___ O2![]() ______SO2+_____Fe2O3
______SO2+_____Fe2O3
(3)实验室常用如图所示实验验证质量守恒定律.四位同学设计了如下A、B、C、D四个实验,并按如图实验操作来验证质量守恒定律,实验中观察到B、C实验前后天平依然保持平衡,某同学认为B、C实验都能验证质量守恒定律,你认为他的说法____ (填“是”或“否”)正确;为什么:_________,C中的现象是:___________。 而A、D实验天平不平衡,其中D实验天平不平衡的原因是____________;并写出C的化学方程式,C______________________,
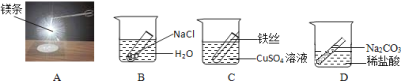
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是甲、乙两同学对镁相关实验的系列研究。
研究一:镁与盐酸反应过程中的能量变化以及反应速率的变化:
(1)反应中试管外壁发烫,说明镁与稀盐酸反应是________反应(填 “吸热”或“放热”)。
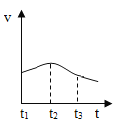
(2)实验测得镁片产生气体的速率(v)与时间(t)的关系如图所示,则t1~t2时间内反应速率逐渐加快的主要原因是__________。镁与盐酸反应的化学方程式:___________。
研究二:反应后所得溶液的酸碱性探究::
(3)甲同学反应后用pH试纸测定试管中溶液的酸碱性,发现pH小于7,说明甲同学所得溶液呈酸性。甲同学:猜想Ⅰ:稀盐酸过量,使溶液呈酸性;猜想Ⅱ:氯化镁溶液呈酸性。为验证猜想,甲同学需测定__________溶液的酸碱性,实验表明该溶液显弱酸性。
(4)乙同学重复甲同学实验时,发现反应后所得试管中溶液pH大于7,说明溶液呈碱性。发现实验与甲同学实验不同的是,反应后的试管中镁条有剩余。乙同学猜想可能是镁与热水反应生成了碱性物质。乙同学为验证猜想,在滴有两滴酚酞的热水中放入一段打磨过的镁条,观察到溶液很快变为红色,同时还观察到镁条表面有气体生成,收集并点燃该气体,发现能燃烧。乙同学查阅资料得知,镁可以与水发生置换反应,请写出镁与水反应的化学方程式_________。
(5)活泼金属能与水在一定条件下反应。实验发现钠与冷水剧烈反应,产生大量的气体。由此可见金属与水反应与金属的活动性顺序________(填“有关”或“无关”)。
研究三:金属活动性强弱与原子结构的关系:

如图为镁原子、钙原子和钡原子结构示意图。已知其中Ba的活动性最强,据此推测,金属的活动性除与原子的最外层电子数有关,还与_________有关。
研究四:确定镁条的成分:
称取3.2g表面被氧化的镁条, 放入100g稀盐酸中恰好完全反应,得到氢气0.2g。求:
(6)此镁条中金属镁的质量为________。
(7)反应后所得溶液中溶质的质量________。氧化镁与稀盐酸能反应,类似盐酸除铁锈的原理。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示。则x=_____;W由_____元素组成;该反应的化学方程式中O2与W化学计量数之比为_____。
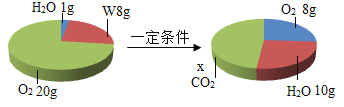
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中常见物质的性质、制法等是化学研究的重要内容。
(1)复分解反应发生后,生成物肯定不会是_________(填“单质”或“化合物”)
(2)盐酸与氢氧化钠溶液反应时溶液pH的变化如下图所示。下列说法正确的是______。
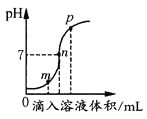
a.m点所示溶液为碱性
b.n点所示溶液中加紫色石蕊溶液显红色
c.p点所示溶液中的溶质为NaCl和NaOH
d.该图所对应操作是将盐酸滴入氢氧化钠溶液中
(3)浓硫酸和浓盐酸敞口放置均会变稀,这是为什么?_________________
(4)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。
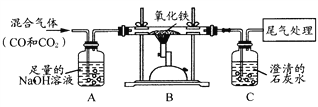
①B装置玻璃管里可观察到的现象为____________________________________。
②C装置中反应的化学方程式为_____________________________。
③实验结束后,若要确定A装置的溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论。(提示:Na2CO3溶液呈碱性)__________
(5)现有73 g溶质质量分数为10%的稀盐酸和127 g氢氧化钠溶液恰好完全反应,求反应后溶液中溶质的质量分数。__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com