
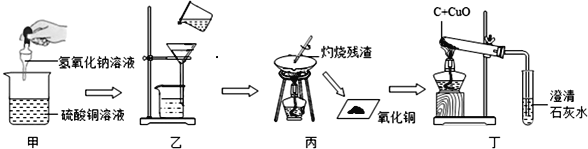
【题目】化学实验技能是学习化学和进行探究活动的基础和保证.某化学兴趣小组进行了一些实验,主要操作过程如图所示:
请回答下列问题:
(1)实验甲中烧杯内的现象是__________;反应的化学方程式为:__________。
(2)实验乙中的一处明显错误是_______________________。
(3)实验丙中使用到了玻璃棒下列实验中必须使用玻璃棒________(填写字母序号)。
A.稀释浓硫酸 B.硫在氧气中燃烧
C.配制6%的食盐水 D.实验室制取二氧化碳
(4)实验丁观察到的现象:______________。
反应的化学方程式为:_______________________。
【答案】 有蓝色沉淀 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 没有用玻璃棒引流 AC 黑色粉末变成红色粉末,澄清石灰水变浑浊 C+2CuO加热2Cu+CO2;CO2+Ca(OH)2= CaCO3↓+H2O
【解析】(1)氢氧化钠溶液可以和硫酸铜反应生成蓝色的氢氧化铜沉淀,发生反应的化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 ;
(2)根据过滤时的操作“一贴二低三靠”可以知道,图中没有用玻璃棒引流;
(3)根据具体的操作过程和方法可以知道:A.稀释浓硫酸时为了使产生的热量及时散失而用玻璃棒来搅拌,故A正确;B.硫在氧气中燃烧,无需用到玻璃棒,故B错误;C.用PH试纸测肥皂水的pH时用玻璃棒蘸取溶液,故C正确;D.实验室制取二氧化碳无需用到玻璃棒,故D错误;故选AC;
(4)丁中将氧化铜和木炭粉混合物加热一段时间,可观察到黑色粉末变成红色粉末,澄清石灰水变浑浊 ,发生反应的化学方程式为C+2CuO![]() 2Cu+CO2、CO2+Ca(OH)2= CaCO3↓+H2O。
2Cu+CO2、CO2+Ca(OH)2= CaCO3↓+H2O。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:初中化学 来源: 题型:
【题目】下图为实验室常用的实验装置。回答问题:

(1)标号仪器的名称:① ;② 。
(2)A、F组合制氧气,氧气收集完毕,应先 (填“熄灭酒精灯”或“从水中取出导气管”)。
(3)用B、D组合制取气体的化学反应方程式 。
若将发生装置由B改为C,其优点是 。
(4)硫化氢气体(H2S)有毒,溶于水形成酸。用块状硫化亚铁(FeS)和稀硫酸发生复分解
反应制得H2S,反应化学方程式为 。某同学用下图G、H 、I组合收集H2S。

①G收集H2S,说明其密度比空气 (填“大”或“小”)。
②各装置的作用:H 、I 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙酰水杨酸(化学式为C9H8O4)也叫阿司匹林,具有解热镇痛作用,下列关于乙酰水杨酸的说法正确的是( )
A.由21个原子构成
B.由碳、氢、氧三个元素组成
C.碳、氢、氧三种元素的质量的质量比为27:2:16
D.属于氧化物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“创建国家卫生城市,建设美好幸福东台”是我们的责任,下列做法不利于环境保护的是
A. 爱护校园花草 B. 大量使用化石燃料
C. 禁止秸秆燃烧 D. 工厂废水达标后排放
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲烷和水反应可以制水煤气,其反应的微观示意图如下所示:
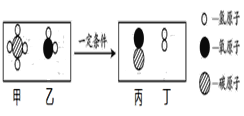
下列对该反应的叙述正确的是
A. 一个甲分子中含有4个原子
B. 该反应中含有一种有机物
C. 反应前后分子数目不变
D. 该反应中,丙和丁的质量比为14:7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化硫(SO2)虽然是一种空气污染物,但也具有一些重要的用途,如漂白剂、防腐剂、制硫酸等。二氧化硫中硫元素的化合价为
A. +1 B. +2 C. +3 D. +4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某固体粉末由Mg、MgO、Mg (OH)2中的一种或几种组成。某化学小组为了探究该固体粉末的成分,设计如图所示的装置(固定装置省略)。
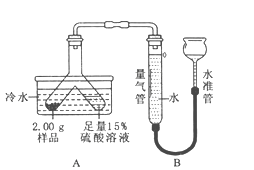
【信息资料】本实验条件下,氢气密度为0.09g/L。
【实验过程】
步骤Ⅰ:检查装置气密性,装入药品并连接仪器。
步骤Ⅱ:倾斜Y形管,使样品充分反应,测的生成气体的探究为55.6mL。
步骤Ⅲ:拆下装置,往Y形管内残余液中加入氢氧化钠溶液,至不再生成沉淀。经过滤、洗涤和干燥后,称得沉淀质量为2.90g。
【回答问题】
(1)该套装置气密性的检验方法是 。
(2)①使样品与硫酸充分反应的正确操作是 (填标号)。
A.硫酸溶液转移到样品中 B.样品转移到硫酸溶液中
②判断样品完全反应的现象是 。
(3)根据实验结果分析:
①通过步骤Ⅱ推断,样品中一定含有的物质是 。
通过步骤Ⅲ计算,样品中镁元素的总质量为 。
②结论:该样品中的成分是 。
【反思】
(4)该化学小组同学经过讨论得出以下结论,正确的是 (填标号)。
A.利用该实验方案,能计算出样品中各物质的质量
B.实验前可通过样品的质量估算硫酸溶液的质量,确保样品完全反应
C.仅称量步骤Ⅱ中Y形管内药品减轻的质量,即能计算出样品中各物质的质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组对热水壶底部水垢的主要成分进行了如下探究,请回答问题。
【查阅资料】天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质——水垢(主要成分为碳酸盐和碱)。有关物质的溶解性见下表。

【提出猜想】水垢的主要成分中一定含有______和_________(填化学式),可能含有Ca(OH)2和MgCO3。
【设计方案】 实验1:确定水垢中是否含Ca(OH)2和CaCO3
实验步骤 | 实验现象 | 结论 |
在少量研碎的水垢中加入适量的蒸馏水充分搅拌,过滤,在滤液中加入Na2CO3溶液。 | 没有白色沉淀产生 | 一定不含 Ca(OH)2 ,一定含 CaCO3 |
实验2:确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究。其主要实验步骤如下:
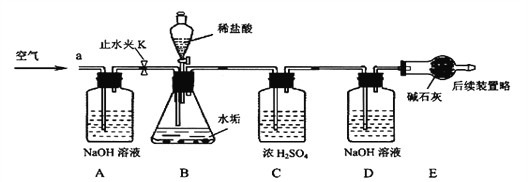
称量D、E装置总质量为600.00g,按上图组装后,将2.50g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为601.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响)。
【实验讨论】(1)加入样品前应_______________________________。
(2)反应结束后打开止水夹K,缓缓鼓入空气的目的是_______________________,装置A的作用是________________________________ 。
(3)A、B装置之间_____设置干燥装置(填:“要”或“不要”),理由是_____________。
(4)装置B中生成CO2的质量为______g。通过计算说明水垢中_____含MgCO3(填字母)。
A. 一定 B. 一定不 C. 可能 D. 无法确定
实验3:确定水垢中是否含有Mg(OH)2
(5)另取质量为2.50g的水垢,加入3.65%的稀盐酸与之反应,测得消耗稀盐酸w g。结合以上实验结论,判断w的值满足________________条件时,水垢中一定含有Mg(OH)2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com