
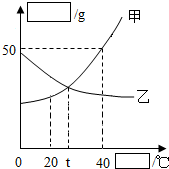
 如图是甲、乙两种物质的溶解度曲线图:
如图是甲、乙两种物质的溶解度曲线图:分析 根据题目信息和溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;根据题意判断,图中的横坐标和纵坐标分别表示温度和溶解度;t℃时,甲、乙两种物质的饱和溶液中的溶质质量分数相等,因为在该温度下的溶解度相等.40℃时,75g甲物质的饱和溶液中,溶剂的质量为50g,因为在该温度下甲物质的溶解度是50g;将20℃时甲的饱和溶液升温至40℃,所得溶液中溶质的质量分数是不变的,因为升温后甲的溶质和溶剂不变.
解答 解:(1)根据题意判断,图中的横坐标和纵坐标分别表示温度和溶解度;故答案为:温度;溶解度;
(2)t℃时,甲、乙两种物质的饱和溶液中的溶质质量分数相等,因为在该温度下的溶解度相等,故答案为:饱和溶液中;
(3)40℃时,75g甲物质的饱和溶液中,溶剂的质量为50g,因为在该温度下甲物质的溶解度是50g;故答案为:75;
(4)将20℃时甲的饱和溶液升温至40℃,所得溶液中溶质的质量分数是不变的,因为升温后甲的溶质和溶剂不变;故答案为:不变;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是“电解水实验”的装置图,根据所学知识回答问题:
如图是“电解水实验”的装置图,根据所学知识回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 溶质 溶剂 | NaOH | Na2CO3 | 固体碘 |
| 酒精 | 不反应,但能溶解形成无色透明溶液 | 不溶也不反应 | 易溶 |
| 水 | 易溶 | 易溶 | 微溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 浓硫酸(H2SO44500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com