
【题目】下列物质露置于空气中,因发生化学变化而使质量增加的是
A.浓硫酸 B.烧碱 C.浓盐酸 D.双氧水
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:
【题目】右图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )

A.甲的溶解度大于乙的溶解度
B.35℃时100g甲的溶液中含甲的质量60g
C.10℃时甲、乙两物质的溶解度相等
D.甲中混有少量乙时可用蒸发结晶的方法提纯甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为实验室常用的实验装置.回答问题:
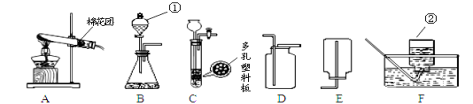
(1)标号仪器的名称:① ;② .
(2)做铁丝在氧气中燃烧实验时应选择的收集装置是 .
(3)用B、D组合制取气体的化学反应方程式 .若将发生装置由B改为C,其优点是 .

(4)硫化氢气体(H2S)有毒,溶于水形成酸.用块状硫化亚铁(FeS)和稀硫酸发生复分解反应制得H2S,反应化学方程式为 .某同学用上图G、H 、I组合收集H2S.
①用G收集H2S,说明其密度比空气 (填“大”或“小”).
②各装置的作用:H 、I .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活、生产、环保等都离不开化学。我们学习了化学知识后,观察物质世界就要从化学视角看。
(1)节假日,某班同学去郊外进行野炊活动。请回答下列问题。
①他们所带的下列物品中,主要材料属于合成高分子材料的是 。(填序号)
A.纯净水 B.棉布围裙 C.铁锅铁铲 D.塑料凳子
②学生野炊食谱如下:主食:馒头;配菜:红烧肉、豆腐汤、牛肉干和黄瓜.你认为食谱中的馒头主要为人体补充的营养素是 。
⑤在引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,其原因是 。
⑥若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),可用下列物质之一涂抹以减轻疼痛,该物质是 。(填序号) A.食醋(pH<7)B.食盐水(pH=7)C.肥皂水( pH>7)
(2)水是生命之源,也是人类最宝贵的资源。试用你学过的化学知识,回答下列问题。
①下图是水分子的电解模型图,根据质量守恒定律可判断该模型图中缺少了 。
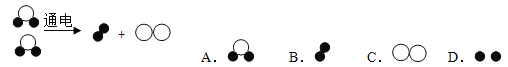
②欲判断得到的生活用水是硬水还是软水,可加入 进行检验,生活中常通过 的方法降低水的硬度。
③水是最重要的溶剂,可以配制不同的溶液。
Ⅰ.20℃时,NaCl 的溶解度是36 g。该温度下,饱和食盐水中溶质与溶剂的质量比为 ;
Ⅱ.某氢氧化钾溶液中,平均每100个水分子中溶有1个钾离子。则这种溶液中氢氧化钾的质量分数约为 。(精确到0.1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通过一年的化学学习,你已经初步掌握了实验室制取气体的一般规律和它们的一些主要性质,以下是老师为你提供的气体制取的实验装置.请你回答下列问题:

(1)写出图中标有字母的仪器名称:a 。
(2)收集得到较纯净的氧气应选用的收集装置是 (选填序号,下同)。
(3)写出一个用A装置或B装置制取氧气的化学方程式: 。
(4)实验室中加热氯化铵和熟石灰的固体混合物制取氨气,应选用的发生装置为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学用量筒量取液体,先仰视读数为19ml,倒出一些液体后,俯视读数11ml。则该同学倒出的液体体积一定 ( )
A.大于8mL B.小于8mL C.无法确定 D.等于8mL
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列对宏观现象的微观解释中错误的是( )
A.变瘪的乒乓球放入热水中能鼓起来,是因为分子受热膨胀变大
B.氧气降温加压后变成液氧,是因为分子间的间隔变小
C.不同的花儿有不同的香味,是因为不同的分子性质不同
D.非吸烟者受到被动吸烟的危害,是因为分子在不断地运动
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如图所示:

已知:王水(王水是浓盐酸和浓硝酸按体积比为3:1混合而成)与FeS2反应的化学方程式:FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)过滤用的玻璃仪器除烧杯、玻璃棒、还有 ;
(2)通常黄铁矿中会含有其它金属杂质,用方法I测定黄铁矿试样中FeS2的含量时,测定结果会 (填“偏高”、“偏低”、“不变”)(测定过程中产生的误差可忽略)。
(3)方法II中加足量BaCl2溶液的作用是 ,写出与氯化钡反应的化学方程式 ;
(4)工业上一般不直接用黄铁矿冶炼铁的原因是: 。
(5)称取黄铁矿试样2.60g,用方法Ⅱ进行测定,称得干燥后的滤渣质量为1.66g,假设矿石中的硫元素全部来自于FeS2,则该矿石中FeS2的质量分数是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com