
| A. | CH3OH | B. | C2H5OH | C. | C6H12O6 |
分析 根据二氧化碳中C的质量分数和二氧化碳的质量,即可算出二氧化碳中含有碳的质量;同理根据水中H的质量分数和水的质量,即可计算出水中含有氢的质量;进而求出碳氢原子个数比,对照选项,选出正确答案.
解答 解:二氧化碳中碳的质量为:8.8g×$\frac{12}{44}$×100%=2.4g;
水中氢的质量为:5.4g×$\frac{2}{18}$×100%=0.6g;
C、H原子个数比为:$\frac{2.4g}{12}:\frac{0.6g}{1}$=1:3;
观察选项,故选B.
点评 本题主要考查学生运用质量守恒定律和化学式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
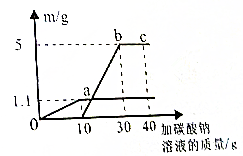 小红取实验时制CO2反应后的废液50g(含有CaCl2和HCl),逐滴加入碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量
小红取实验时制CO2反应后的废液50g(含有CaCl2和HCl),逐滴加入碳酸钠溶液.他根据实验测得的数据绘出如图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液质量查看答案和解析>>
科目:初中化学 来源: 题型:填空题
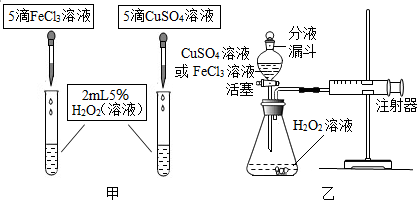
| 实验操作 | 实验现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
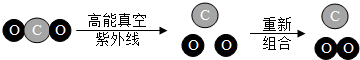
| A. | 属于分解反应 | B. | 反应中的最小微粒是分子 | ||
| C. | 符合质量守恒定律 | D. | 为制取氧气提供了新方法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com