
【题目】下列物质俗名与化学式相对应的是
A. 纯碱—NaOH B. 酒精—C2H6O C. 小苏打—Na2CO3 D. 生石灰—Ca(OH)2
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:
【题目】2014年4月14日,科学家约翰帕特森向人们展示了一款真正意义上的原子手表,它内置了一 个芯片级的铯原子钟,每1000年仅有1秒的误差.已知这种铯原子核内质子数为55,相对原子质量为133,则其核外电子数为
A. 188 B. 78 C. 55 D. 23
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类宝贵的自然资源。
(1)天然水中含有许多杂质,实验室常用过滤方法除去水中不溶性杂质,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和 (填仪器名称)。
(2)硬水给生活和生产带来很多麻烦,生活中常用 的方法降低水的硬度。
(3)氯气可用作自来水的消毒剂,实验室制取氯气的化学方程式为:MnO2 + 4HCl(浓)![]() X +Cl2 ↑ + 2H2O , X的化学式为 。
X +Cl2 ↑ + 2H2O , X的化学式为 。
(4)在电解水的实验中,两电极相连的玻璃管上方产生的气体是氧气和氢气,一段时间后,氧气和氢气的体积比约为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、B、C、D、E是初中化学中五种常见的纯净物,五种物质中只有A为黑色其余都为无色,A、E为单质其余都为化合物, B、C所含元素相同,相对分子质量:C>B>D=18;由于条件不同A和E反应可生成B也可生成C。五种物质在一定条件下的转化关系如图所示(“—”表示相连物质间能反应,“→”表示物质间可转化,部分反应物和生成物没有列出)。试推断并回答相关问题:
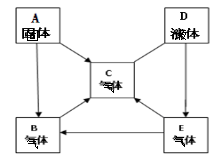
(1)A的化学式是 ;B的化学式是 。
(2)C、D发生化合反应的化学方程式是 。
(3)D→E的化学反应方程式是 。
(4)气体B的一种化学性质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法不正确的是
A. 误食重金属盐,可服牛奶或鸡蛋清解毒
B. 水中Ca2+、Mg2+的增多会促进人体健康
C. 米饭遇到大量加碘食盐不会逐渐出现蓝色
D. 羊毛在空气中灼烧产生烧焦羽毛的气味
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】早在春秋战国时期,我国就开始生产和使用铁器。工业炼铁把铁矿石和焦炭、石灰石一起加入高炉,在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
一氧化碳还原氧化铁的化学方程式为: 。其中,石灰石起的作用是 。
(一)甲组同学在学习炼铁的相关内容时,对炼铁时还原剂的选择进行了如下探究。
【提出问题】
单质碳也具有还原性,碳还原氧化铁的化学方程式为 。为什么工业上不用焦炭作为还原剂直接还原铁矿石?
【猜想与假设】
焦炭和铁矿石都是固体,接触面积小,反应不易完全。
【进行实验】
①称取两份相同质量的氧化铁粉末。一份与足量的碳粉均匀混合放入图1装置A的试管中;另一份放入图1装置B的玻璃管中。
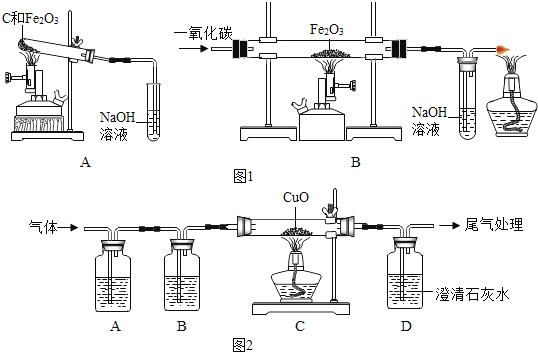
②图1装置A和B两组实验同时开始进行。在图1装置B的反应中,实验开始前应先 (选填“通CO”或“加热”); 实验结束后应继续通入CO直至冷却至室温,其原因是 。
【实验现象】
当图1装置B的玻璃管中固体完全由 时(选填“红色变为黑色”或“黑色变为红色”),图1装置A的试管中仍有 。
【解释与结论】
焦炭和铁矿石都是固体,接触面积小,反应确实不易完全,这可能是工业上不用焦炭作为还原剂直接还原铁矿石的一个原因。
【完善实验】
联想到单质碳的一些化学性质,甲同学认为在碳还原氧化铁的反应中可能还会有CO产生。为了证明碳还原氧化铁所得的气体中含有CO和CO2,将该气体通过图2的检验装置。图2A装置中的试剂是(写名称,下同) ,图2B装置中的试剂是氢氧化钠溶液,用以吸收二氧化碳(2NaOH+CO2═Na2CO3+H2O );证明原混合气体中CO2存在的化学方程式 ;证明原混合气体中CO存在的实验现象是 ;经过检验,证实碳还原氧化铁所得的气体中确实含有CO和CO2。
(二)精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】
利用绿矾制备精还原铁粉的工艺流程如下:
![]()
粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为
FexOy+yH2![]() xFe+yH2O,Fe3C+2H2
xFe+yH2O,Fe3C+2H2![]() 3Fe+CH4。
3Fe+CH4。
【含量测定】
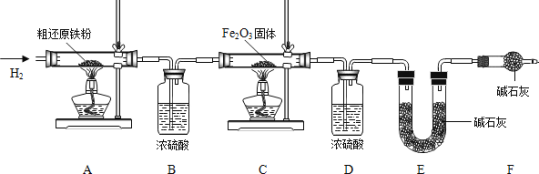
为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按图装置进行实验。
已知3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe(假设每步反应都完全,且不考虑装置内原有空气对测定结果的影响)。
(1)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃酒精灯, (填“先点A处,后点C处”或“先点C处,后点A处”);
④分别熄灭A处、C处酒精灯;
⑤再缓缓通入少量H2;
⑥再次称量必要装置的质量
(2)步骤②的目的是 ,验证该步骤目的达到的实验方法是 ;
(3)若缺少装置D,则所测氧元素的质量分数将 (填“偏大”,“偏小”或“不变”)。
(4)粗还原铁粉样品的质量为15.000g,装置B、E分别增重0.270g和0.330g,则计算样品出中碳、氧元素的质量分数分别是 。(列出计算过程,2分)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com