


科目:初中化学 来源: 题型:
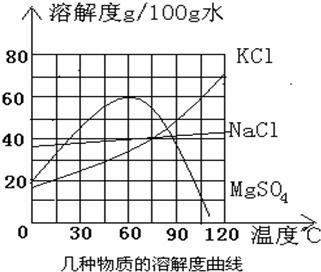 海水日晒后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含氯化镁、硫酸镁、氯化钾,在食品、化工等方面有重要应用.氯化镁在不同温度下的溶解度表
海水日晒后得到的晶体是粗盐,剩余的液体称为苦卤,苦卤中除氯化钠外还含氯化镁、硫酸镁、氯化钾,在食品、化工等方面有重要应用.氯化镁在不同温度下的溶解度表| 温度℃ | 0 | 60 | 90 | 120 |
| 溶解度(g/100g水) | 50 | 60 | 70 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:
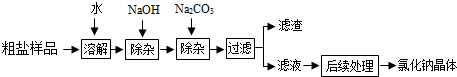
查看答案和解析>>
科目:初中化学 来源: 题型:
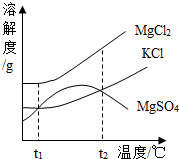
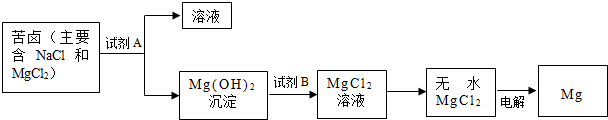
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
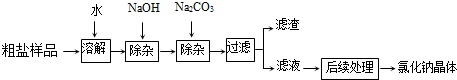
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com