
【题目】甲、乙两种固体(不含结晶水)的溶解度曲线如图所示。下列说法正确的是
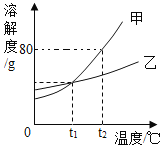
A. t1℃时,甲、乙饱和溶液溶质的质量分数相等
B. 乙中含有少量甲时,可用降温结晶法提纯乙
C. t2℃时,将50g甲加入50g水中,可得到100g溶液
D. t2℃时的甲、乙饱和溶液分别降温到t1℃时,析出晶体的质量甲大于乙
【答案】A
【解析】
根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
A、根据溶解度曲线可知,t1℃时,甲、乙溶解度相等,则甲、乙饱和溶液溶质的质量分数相等,故选项正确;
B、据图可以看出,甲的溶解度随温度的升高变化比乙明显,乙中含有少量甲时,可用蒸发结晶的方法提纯乙,故选项不正确;
C、t2℃时,甲的溶解度为80g,故将50g甲加入50g水中,只能溶解40g,可得到90g溶液,故选项不正确;
D、t2℃时,分别将甲、乙的饱和溶液降温至t1℃,由于溶液质量不确定,不能确定析出晶体质量大小,故选项不正确;
故选A。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】 工业盐酸中通常含少量FeC13而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸50g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表,请根据表格和图象完成下列问题:
加入NaOH溶液的质量/g | 25 | 50 | 75 | 100 |
所得溶液的质量/g | 75 | 100 | 125 | m |

(1)开始没有产生沉淀的原因是_____。
(2)求该工业盐酸中HCl的质量分数______(写出计算过程)。
(3)m=_____(结果保留两位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象不能正确反映对应变化关系的是( )
A. 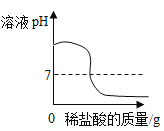 向盛有NaOH溶液的烧杯中滴加稀盐酸
向盛有NaOH溶液的烧杯中滴加稀盐酸
B. 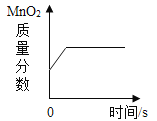 加热氯酸钾和二氧化锰的固体混合物
加热氯酸钾和二氧化锰的固体混合物
C. 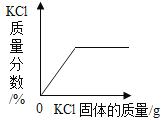 在一定温度下,向接近饱和的氯化钾溶液中加入氯化钾固体
在一定温度下,向接近饱和的氯化钾溶液中加入氯化钾固体
D. 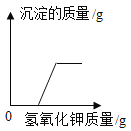 向盐酸和氯化镁的混合溶液中滴加氢氧化钾溶液
向盐酸和氯化镁的混合溶液中滴加氢氧化钾溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室配制饱和澄清石灰水和质量分数为10%的氢氧化钠溶液,并进行有关实验。
下表是20℃时部分物质的溶解度数据。
物质 | Ca(OH)2 | NaOH | CaCO3 | Ca(HCO3)2 | Na2CO3 | NaHCO3 |
溶解度/g | 0.16 | 109 | 0.0065 | 16.6 | 21.8 | 9.6 |
(1)配制溶液。其中配制100g10%氢氧化钠溶液的基本步骤是:
称取氢氧化钠固体—量取水—溶解—装瓶贴标签。

①称取氢氧化钠固体的质量_____________g。
②已知水的密度为1g/cm3,用100mL量筒量取所需的水,_______画出水的液面。
③装瓶后贴标签,在标签上填写:_______________________________。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向饱和澄清石灰水中通入CO2直至过量,先生成CaCO3,再转化为Ca(HCO3)2,可观察到的现象是________________________________。
②向10%氢氧化钠溶液中通入CO2直至过量,先生成Na2CO3,再转化为NaHCO3,可观察到的现象是_______________________________________________________。
③理论上吸收4.4gCO2,需饱和澄清石灰水的质量至少为___________g,或需10%氢氧化钠溶液的质量至少为__________g。(计算结果精确到个位)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将黑色固体粉末A与白色晶体B混合加热,可产生无色气体C,而黑色固体粉末A在反应前后的质量和化学性质都不变。氢气在无色气体C中可以燃烧,生成D,D通常是液态,是生物体内含量最多的物质。
(1)写出B的名称_____;D的化学符号:_____
(2)写出氢气在C中燃烧的文字表达式:_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图像如下:
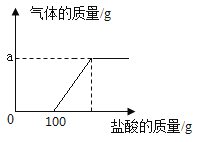
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 | 50 |
烧杯中物质的质量/g | 100 | 150 | 197.8 | 245.6 | 295.6 |
请根据有关信息计算:
(1)a的数值为________。
(2)稀盐酸中溶质的质量分数为_____。(写出计算过程)
(3)恰好完全反应后所得溶液中溶质的质量为_____。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_____,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
(实验用品)pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(猜想与假设)反应后溶液中溶质的可能组成成分。
猜想一:硫酸钠
猜想二:硫酸钠、碳酸氢钠
猜想三:硫酸钠、硫酸
(实验探究)同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成如表实验现象中的空格。
实验方案 | A | B | C | D |
实验操作 |
|
|
|
|
实验现象 | _____ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH<7 | _____ |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
(得出结论)猜想三正确。
(评价反思)
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显的操作错误是_____。
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由_____。
(总结提高)依据所给实验用品,设计与上述实验不同的方案,确认猜想三是正确的,请你写出你的实验方案_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表的部分信息,请根据下表回答有关问题:
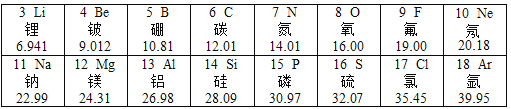
(1)具有相似化学性质的一组元素是_____。
A.Na、Cl B.C、Be C.F、Cl D.Cl、Ar
(2)由第7号元素和第12号元素的原子形成化合物的化学式为_____。
(3)某粒子的结构示意图如图,当x﹣y=8时,该粒子的符号为_____。
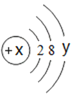
(4)钠、氯、氧三种元素可形成原子个数比为1:1:4的化合物,则此化合物中氯元素的化合价为_____。
(5)具有相同原子数和电子数的分子或离子叫等电子体。下列各组粒子中属于等电子体的是_____。
A.NO和O2 B.CO和N2 C.SO2和CO2 D.NH4+和H2O
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】合成氨是人类科学技术上得一项重大突破,对社会发展与进步做出了巨大贡献.合成氨的工艺流程图 如下:
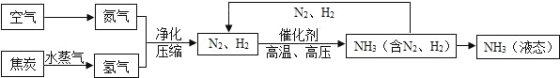
(1)合成氨需要的氮气来自空气,空气中氮气的体积分数约为_____.
(2)制取氢气的反应过程为:C+H2O![]() CO+H2,CO+H2O
CO+H2,CO+H2O![]() CO2+H2.上述两个化学方程式中表现 氧化性的物质是_____(填化学式).
CO2+H2.上述两个化学方程式中表现 氧化性的物质是_____(填化学式).
(3)原料中 N2、H2 中常含有 CO2 和水蒸气,反应前要净化.净化的过程是_____.
(4)写出 N2、H2 反应生成 NH3 的化学方程式_____.
(5)将沸点不同的气体分离开来,常采用液化分离法.如,控制温度在﹣183℃时,可将空气中 N2 与 O2分离.根据表中物质的沸点判断,要将产物 NH3 与 N2 、H2 分离开来,最适宜的温度应该控制在___℃
物质 | H2 | N2 | O2 | NH3 |
沸点 | ﹣252℃ | ﹣195.8℃ | ﹣183℃ | ﹣33.35℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com