
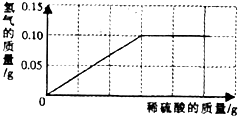
 为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品
为了测定黄铜(铜、锌合金)的组成,某研究性学习小组称取该样品分析 根据锌与硫酸反应的化学方程式,由图中最多生成的氢气质量0.10g,可以计算出:
(1)参加反应的锌的质量,进而计算出样品中铜的质量分数;
(2)参加反应硫酸的质量,进而计算出硫酸溶液的质量;
(3)根据质量守恒定律可求出反应后所得溶液质量.
解答 解:(1)设样品中锌的质量为x;消耗稀硫酸中溶质的质量为y.
Zn+H2SO4═ZnSO4+H2↑
65 98 2
x y 0.10g
$\frac{65}{x}=\frac{98}{y}=\frac{2}{0.1g}$ x=3.25g,y=4.9g,z=6.8g
样品中铜的质量分数为:$\frac{10g-3.25g}{10g}$×100%=67.5%
(2)反应所消耗的硫酸溶液质量为:$\frac{4.9g}{9.8%}$=50g
(3)所得溶液的溶质质量为:50g+3.25g-0.1g=53.15g
答:(1)样品中铜的质量分数为67.5%;
(2)消耗硫酸溶液的质量为50g;
(3)所得溶液的溶质质量为53.15g.
点评 本题主要考查有关化学方程式的计算和质量分数的计算,难度较大.计算所得溶液质量时,要注意:①不能把铜的质量计算在所得溶液中;②不能把生成氢气的质量计算在所得溶液中.


科目:初中化学 来源: 题型:选择题
| A. | 醋酸、甲酸、CH3COOH、酸 | B. | 氢氧化钠、苛性钠、NaOH、碱 | ||
| C. | 氢氧化钙、生石灰、Ca(OH)2、碱 | D. | 碳酸钠、纯碱、NaCO3、盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3→Na2SO4 | B. | NH4NO3→NH3 | C. | Fe2O3→FeCl2 | D. | NaOH→Cu(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶质可以是固体、液体、气体 | |
| B. | 溶液都是均-、稳定的混合物 | |
| C. | 同种溶质的饱和溶液,一定比它的不饱和溶液的浓度大 | |
| D. | 析出晶体后的溶液一定是该温度下的饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
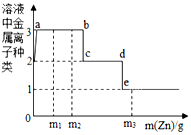 某溶液含有硝酸铜和硝酸银,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系(如图所示).下列说法不正确的是( )
某溶液含有硝酸铜和硝酸银,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系(如图所示).下列说法不正确的是( )| A. | a-b间(不含两点)的溶液中金属离子为Zn2+、Ag+、Cu2+ | |
| B. | c-d间(不含两点)的溶液中金属离子为Zn2+、Cu2+ | |
| C. | 当参加反应的锌的质量为m2时,溶液中金属离子为Zn2+ | |
| D. | 当参加反应的锌的质量分数为m1、m2时,溶液中的硝酸铜质量分数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com