
 如图是A、B、C三种物质的溶解度随温度变化的曲线图,根据图回答下列问题:
如图是A、B、C三种物质的溶解度随温度变化的曲线图,根据图回答下列问题:| 2g |
| 2g+10g |


科目:初中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论 | |
| 甲同学 | 取烧杯中溶液少许于试管中,向其中滴加 |
现象:溶液变为红色 | 溶液显酸性(含有H+);溶质中有氯化氢. |
| 乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象: 反应的化学方程式是: | |
| 丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量石灰石 | 现象: |
查看答案和解析>>
科目:初中化学 来源: 题型:
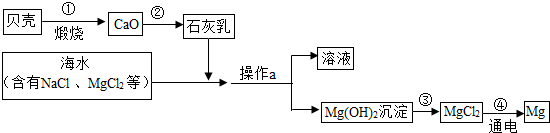
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
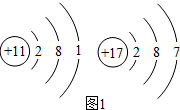 我们的日常生活离不开食盐,食盐的主要成分是氯化钠.
我们的日常生活离不开食盐,食盐的主要成分是氯化钠.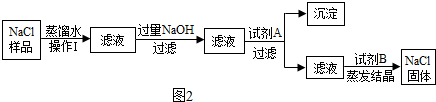
查看答案和解析>>
科目:初中化学 来源: 题型:
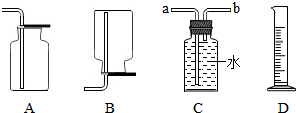 回收废旧干电池能减少对水和土壤的污染.某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图.
回收废旧干电池能减少对水和土壤的污染.某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图.| 实验编号 | 试剂 | H2体积(mL)(均收集10分钟) | |
| 不同纯度的锌 (均取1g) | 不同浓度的稀硫酸(均取30mL ) | ||
| ① | 纯锌 | 30% | 564.3 |
| ② | 含杂质的锌 | 30% | 634.7 |
| ③ | 纯锌 | 20% | 449.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com