
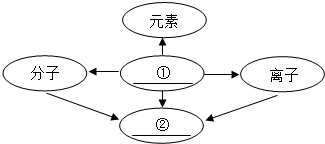
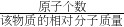 ×100%
×100% ×100%=52.9%,铝元素全部以氧化铝的形式出现,则地壳中氧化铝的质量分数是:7.73%÷52.9%=14.6%
×100%=52.9%,铝元素全部以氧化铝的形式出现,则地壳中氧化铝的质量分数是:7.73%÷52.9%=14.6% 2CO2+3H2O
2CO2+3H2O

 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
 33、构建知识网络是一种重要的学习方法.如图是关于盐酸化学性质的知识网络,“--”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.A、C属于不同类别的化合物.完善这个知识网络.
33、构建知识网络是一种重要的学习方法.如图是关于盐酸化学性质的知识网络,“--”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.A、C属于不同类别的化合物.完善这个知识网络.查看答案和解析>>
科目:初中化学 来源: 题型:
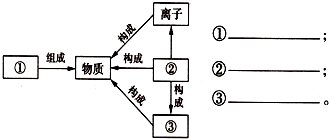
 构建知识网络是一种重要的学习方法.小李同学对物质的组成和结构方面的知识进行了归纳,请你填写空白,完成他的设计.
构建知识网络是一种重要的学习方法.小李同学对物质的组成和结构方面的知识进行了归纳,请你填写空白,完成他的设计.查看答案和解析>>
科目:初中化学 来源: 题型:
 18、构建知识网络是一种重要的学习方法.小李同学对物质组成和结构方面的知识进行了归纳,请你填写空白,完成他的设计.
18、构建知识网络是一种重要的学习方法.小李同学对物质组成和结构方面的知识进行了归纳,请你填写空白,完成他的设计.查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?乌鲁木齐)构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A,B,C分别属于不同类别的化合物,则A,B,C可能是( )
(2013?乌鲁木齐)构建知识网络是一种重要的学习方法.如图是关于硫酸化学性质的知识网络:“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质,A,B,C分别属于不同类别的化合物,则A,B,C可能是( )查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com