
| A. | 28% | B. | 42% | C. | 54% | D. | 64% |
分析 设反应后该混合气体的质量为100g.则混合气体中含碳元素12g,假设甲烷燃烧完全生成二氧化碳和水,求出此时氮气的质量,假设甲烷燃烧完全生成一氧化碳和水,求出此时氮气的质量,氮气的质量应在共同区间内.
解答 解:
设反应后该混合气体的质量为100g.则混合气体中含碳元素12g,则原来甲烷的质量就为12g÷$\frac{12}{16}$=16g,甲烷中氢元素的质量为16g-12g=4g,所以生成水的质量为4g÷$\frac{2}{18}$=36g;所以反应前混合气的质量为100g+36g=136g.
第一种情况:假设甲烷燃烧完全生成二氧化碳和水:
则二氧化碳的质量为12g÷$\frac{12}{44}$=44g,此时假设氧气完全反应,剩余的都是氮气,则氮气的质量为100g-44g=56g,这样氮气的在反应前的混合物中最大质量分数为$\frac{56g}{136g}$×100%=41.2%.而如果剩余气体中只有氧气,则氮气的质量分数为0,所以氮气的质量分数介于0~41.2%之间.
第二种情况:假设甲烷燃烧完全生成一氧化碳和水:
则一氧化碳的质量为12g÷$\frac{12}{28}$=28g,此时假设氧气完全反应,剩余的都是氮气,则氮气的质量为100g-28g=72g这样氮气的在反应前的混合物中最大质量分数为$\frac{72g}{136g}$×100%=52.9%.而如果剩余气体中只有氧气,则氮气的质量分数为0,所以氮气的质量分数介于0~52.9%.
由于CH4全部转化为CO、CO2和H2O,也就是同时又二氧化碳和一氧化碳,则反应前的氮气的质量分数应该是在0~41.2%之间.
故选A.
点评 本题是一道考查混合物质中根据某元素的质量分数来求的另外几种物质或者元素的质量分数,方法有多种,但可以用排除法做类似的题目;难度较大,培养学生的创新和逆向思维能力.


科目:初中化学 来源: 题型:实验探究题
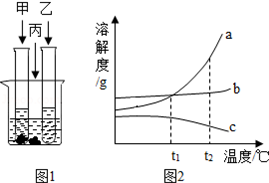
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
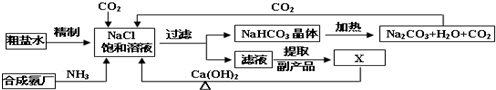
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 提取青蒿素不宜在高温下进行 | |
| B. | 青蒿素是由碳、氢、氧三种元素组成的 | |
| C. | 青蒿素是由C15H22O5分子构成的 | |
| D. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 实验Ⅰ:实验室制O2.
实验Ⅰ:实验室制O2.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
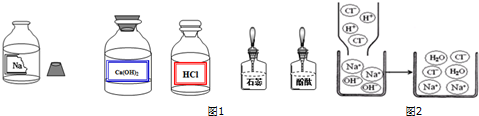
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com