
| A. | 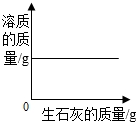 如图是向一定量的饱和石灰水中不断加入生石灰 | |
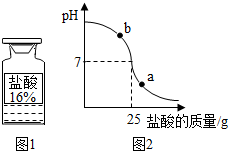
| B. | 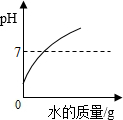 如图是向盛有一定量浓硫酸的烧杯中加入水 | |
| C. | 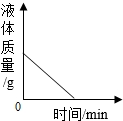 如图是向一定量的氢氧化钠溶液中不断通入CO2 | |
| D. |  如图是向一定量的实验室制取CO2后残留的酸性废水中加入过量Na2CO3溶液 |
分析 A、根据氧化钙与水的反应解答;
B、根据硫酸稀释过程中溶液的pH变化解答;
C、根据氢氧化钠和二氧化碳的反应解答;
D、根据制取二氧化碳的残留酸性液体中含有盐酸和氯化钙解答.
解答 解:A、向一定量的饱和石灰水中不断加入生石灰,则生石灰氧化钙与水反应生成氢氧化钙,由于水被消耗,故饱和溶液中的氢氧化钙会析出,溶质质量减小,错误;
B、向盛有一定量浓硫酸的烧杯中加入水,溶液的pH不会大于7,错误;
C、向一定量的氢氧化钠溶液中不断通入CO2,二氧化碳与氢氧化钠反应生成易溶于水的物质,故溶液的质量增加,错误;
D、向一定量的实验室制取CO2后残留的酸性废水中加入过量Na2CO3溶液,剩余的酸性溶液中含有盐酸和氯化钙,加入的碳酸钠首先与盐酸反应,当盐酸耗尽,氯化钙与碳酸钠反应生成碳酸钙沉淀,图象正确;
故选D.
点评 本题考查的是常见的化学反应与图象的关系,完成此题,可以依据已有的知识进行.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
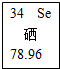 硒在光照下导电能力提高近千倍,因此硒被广泛的用于静电复印机的为感光器(硒鼓),硒鼓的好坏决定了打印机质量.元素周期表“硒”的信息如图所示.下列关于硒元素说法错误的是( )
硒在光照下导电能力提高近千倍,因此硒被广泛的用于静电复印机的为感光器(硒鼓),硒鼓的好坏决定了打印机质量.元素周期表“硒”的信息如图所示.下列关于硒元素说法错误的是( )| A. | 是非金属元素 | B. | 相对原子质量为78.96g | ||
| C. | 原子序数为34 | D. | 元素符号为Se |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | O2 | CO2 | H2O |
| 反应前质量/g | 23 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 27 |
| A. | 该反应为分解反应 | |
| B. | 反应生成的CO2和H2O的质量比为45:27 | |
| C. | 表中“待测”值为22 | |
| D. | 不能确定x中是否含有氧元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com