如图为实验室制备和收集气体的装置图,据图回答问题:
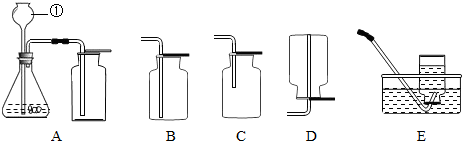
(1)写出①的仪器名称
长颈漏斗
长颈漏斗
.
(2)我们知道有两种气体在实验室可以采用上图装置进行制取,请写出这两个制备反应的化学方程式
、
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.这两种气体可采用相同的收集方法是
向上排空气法
向上排空气法
.
(3)请选择上述两种气体的一种进行验满的实验,其方法是
用带火星的木条放在集气瓶口,若立即复燃则O2已满
(或“用燃着的木条放在集气瓶口,若立即熄灭则CO2已满”)
用带火星的木条放在集气瓶口,若立即复燃则O2已满
(或“用燃着的木条放在集气瓶口,若立即熄灭则CO2已满”)
.
(4)上述两种气体中有一种可与水反应的化学方程式是
H2O+CO2=H2CO3
H2O+CO2=H2CO3
,检验这个反应确实发生方法是
向反应后溶液中滴入紫色石蕊溶液,溶液变红
向反应后溶液中滴入紫色石蕊溶液,溶液变红
.
(5)诺贝尔奖得主穆拉德教授在《神奇的一氧化氮》书中提出:“人体中99.9%的疾病与一氧化氮有关”.已知一氧化氮气体难溶于水,常温下极易与氧气反应,现在实验室中要收集一瓶制备的一氧化氮,选用的装置是
E
E
(选填序号).




