
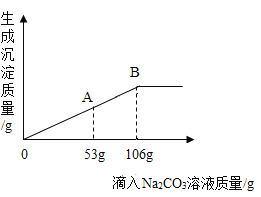
【题目】在一烧杯中盛有一定质量的BaC03固体,向其中加入溶质 质量分数为10%的稀盐酸,至恰好完全反应,得到113.7g不饱和溶液,想所得溶液中逐滴加入质量分数为10%的Na2CO3溶液,生成沉淀质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意回答问题:
(1)在加入稀盐酸的过程中,观察到的明显实验现象是____________ 。
(2)当加入Na2CO3溶液至图中A点时,烧杯中溶液里含有的溶液质是____________(写化学式)。
(3)当加入Na2CO3溶液至图中B点时,求此时所得不饱和溶液的质量__________。
【答案】固体溶解,产生气泡 BaCl2、NaCl 200g
【解析】
碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳,氯化钡和碳酸钠反应生成碳酸钡沉淀和氯化钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断。
解:(1)在加入稀盐酸的过程中,观察到的明显实验现象是固体溶解,产生气泡;
(2)当加入Na2CO3溶液至图中A点时,烧杯中溶液里含有的溶质是碳酸钡和稀盐酸反应生成的氯化钡和氯化钡与碳酸钠反应生成的氯化钠;
(3)设反应生成碳酸钡沉淀的质量为x,
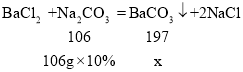
![]()
x=19.7g,
当加入Na2CO3溶液至图中B点时,此时所得不饱和溶液的质量为:113.7g+106g-19.7g=200g;
答:此时所得不饱和溶液的质量为200g。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:初中化学 来源: 题型:
【题目】下表是元素周期表中的1~18号元素原子核外电子排布,我们对它进行研究:
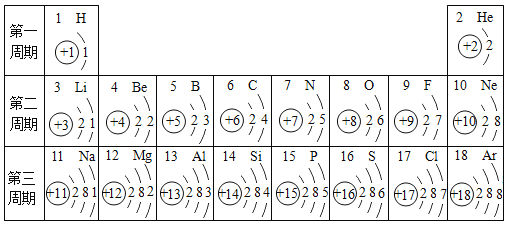
(1)从原子结构上分析,图中氧、硫元素具有相似化学性质的主要原因是 ;
(2)写出质子数为1、6、8、11四种元素组成的可以治疗胃酸过多物质的化学式: 。
(3)![]() 表示一种元素的两种粒子,它们属于同一种元素的依据是 。
表示一种元素的两种粒子,它们属于同一种元素的依据是 。
(4)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学来源于生活,化学与生活密切相关。
(1)电解水过程中不变的微粒是_____(填化学用语),写出该反应的化学方程式_____。
(2)农业生产中,如果农作物缺少钾元素,会出现_____(填序号)。
A 叶色不浓绿 B 茎杆不粗壮 C 根系不发达
(3)铁制品锈蚀的过程,实际上是铁跟空气中的_____发生化学反应的过程;可用稀硫酸除去其表面的铁锈,反应的化学方程式为_____
(4)自来水是通过水厂生产出来符合相应标准的供人们生活、生产使用的水。其生产过程中加入液氯的作用为_____。
(5)铝合金可用于制造飞机的外壳, 铝合金属于_____材料
(6)锰钢属于铁合金,可用于制造钢轨。已知锰的金属活动性介于镁与锌之间,如果用实验比较铁和锰的金属活动性强弱,下列所给试剂组能够达到目的的是_____(填字母序号)。
A Fe、Mn、10%硫酸溶液 B Fe、Mn、MgSO4溶液
C Fe、Mn、ZnSO4溶液 D Cu、FeSO4溶液、MnSO4溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某兴趣小组设计的四个实验装置示意图,其中能够达到实验目的是( )
A. 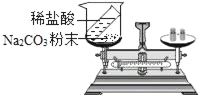 探究质量守恒定律
探究质量守恒定律
B. 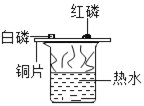 探究燃烧的三个条件
探究燃烧的三个条件
C. 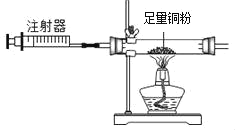 测定空气中氧气的含量
测定空气中氧气的含量
D. 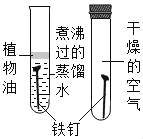 探究铁生锈的条件
探究铁生锈的条件
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】活动探究一:如图是初中化学部分重要实验的装置图,试回答下列问题:

(1)图甲中装置①可用来实验室制取某些气体,写出一个制取气体的化学方程式_____;欲用装置②排空气法收集二氧化碳,则气体应从_____(选填“a”或“b”)端通入.
(2)图乙中实验①的明显错误是_____;②中玻璃棒的作用是_____.
(3)图丙是模拟工业炼铁的实验装置,装置后面气球的作用是_____.
活动探究二:根据下列两组实验回答问题

(1)指出a实验中不正确的操作:_____.
(2)b实验中,正确的操作顺序为(填序号)⑤→_____→②.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如下图所示的实验,回答下列问题。
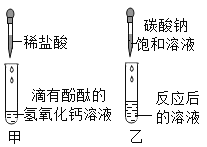
(1)说明甲试管中发生反应的现象。_____
(2)实验结束后,同学们将反应后的溶液中加入碳酸钠溶液,观察到有气泡产生。则反应后的溶液中的溶质是什么_____?这种液体需要加入过量的什么试剂处理后才可以再排放?_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后通入足量NH3和CO2制备NaHCO3,化学方程式:NaCl+ NH3+CO2+H2O= NaHCO3↓+NH4Cl
某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题:
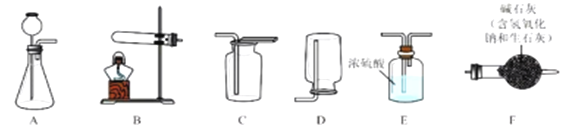
I.气体制备
(1)二氧化碳气体制备
实验室常采用石灰石与稀盐酸反应制备CO2,其化学方程式为_____________。应选择的气体收集装置为______(选填装置对应的字母)。
(2)氨气制备
实验室常用硫酸吸收氨气,防止污染空气,实验室制备NH3的反应原理为:Ca(OH)2(固)+2NH4Cl(固) ![]() CaCl2+2H2O+2NH3↑。现要制备并干燥NH3,所选装置的正确连接顺序为_____→______(选择装置对应的字母)。实验室制备O2也可用上述制备NH3的发生装置,写出用该发生装置制备O2的化学方程式__________。
CaCl2+2H2O+2NH3↑。现要制备并干燥NH3,所选装置的正确连接顺序为_____→______(选择装置对应的字母)。实验室制备O2也可用上述制备NH3的发生装置,写出用该发生装置制备O2的化学方程式__________。
II.NaHCO3制备
物质 | NaHCO3 | NH4Cl |
溶解度/g(20℃) | 9.6 | 37.2 |
(3)根据表格中的溶解度数据,解释20℃产物中NaHCO3能够先从溶液中结晶析出的原因________。
(4)该过程中另一产物NH4Cl在农业生产中常被用作______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图中的物质为初中化学常见物质,它们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物或反应条件已略去)。甲与A溶液反应得到浅绿色溶液;A、B发生中和反应,产物之一是厨房内常用的调味品;C常用于改良酸性土壤,且C的溶液与D的溶液反应可得到B;C与乙混合可配制波尔多液;乙与丙两种溶液反应生成两种不同颜色的沉淀。请回答:

(1)物质丙的化学式是_____;
(2)欲通过一步实验证明A、B是否恰好完全反应,需要向A、B反应后的溶液中加入的试剂是_____;
(3)E→C反应的化学方程式是_____;
(4)甲和乙反应的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是
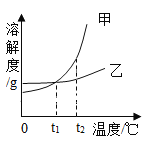
A.甲的溶解度比乙的大
B.t1℃的甲、乙饱和溶液升温至t2℃仍为饱和溶液
C.将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法
D.将甲、乙的饱和溶液从t2℃降到t1℃,所得溶液中溶质的质量分数相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com