
【题目】某小组探究硫酸铜晶体(CuSO4·5H2O)热分解的产物。
(1)加热过程中观察到___色固体先变成白色,再变为黑色,同时闻到刺激性气味的气体
(问题)刺激性气味的气体是什么?
(猜想)猜想1:SO2 猜想2 :SO3 猜想3 :___
(实验1)在老师指导下,小组同学称取24.0g无水CuSO4,加热,充分反应后得到12.0g氧化铜,将生成的气体依次通入①足量稀HCl和BaCl2的混合溶液②酸性高锰酸钾溶液③足量NaOH溶液。
(2)①中出现白色沉淀,则猜想 ______不成立;②中出现 _______(填现象),则猜想3成立。
(3)③能起到吸收尾气的作用,反应的化学方程式为_________
(质疑)无水CuSO4分解除了生成刺激性气味的气体外,是否还有其他气体生成?
(实验2)测定实验1中①得到的沉淀质量为23.3g,②和③共增重3.2g。
(分析)(4)通过计算可以得出,气体中还有____________。
(5)写出实验1中无水CuSO4分解的化学方程式______________。
【答案】蓝 SO2 和 SO3 1 高锰酸钾溶液褪色 2NaOH+SO2=Na2SO3+H2O O2 ![]()
【解析】
二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,三氧化硫能与氯化钡溶液反应生成硫酸钡白色沉淀和盐酸。
(1)硫酸铜晶体(CuSO4·5H2O)是蓝色的,加热过程中观察到蓝色固体先变成白色,再变为黑色,同时闻到刺激性气味的气体。
[猜想] 由质量守恒定律可知,产生的有刺激性气味的气体是二氧化硫,或三氧化硫,或二氧化硫与三氧化硫的混合物,故猜想1:SO2 猜想2 :SO3 猜想3 :SO2 和 SO3。
[实验1](2)三氧化硫能与氯化钡溶液反应生成硫酸钡白色沉淀和盐酸,由①中出现白色沉淀可知,刺激性气味的气体中一定含有三氧化硫,①中出现白色沉淀,则猜想1不成立;二氧化硫有还原性,能使酸性高锰酸钾溶液褪色,所以②中出现高锰酸钾溶液褪色的现象,说明气体中还含有二氧化碳,即为二氧化硫和三氧化硫的混合气体,则猜想3成立。
(3)二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,③能起到吸收尾气的作用,反应的化学方程式为2NaOH+SO2= Na2SO3+H2O。
[分析](4)由质量守恒定律可知,硫酸铜中铜元素的质量与氧化铜中铜元素的质量相等;硫酸铜中硫元素的质量与二氧化硫、三氧化硫中硫元素的质量之和相等。
24.0g无水CuSO4中含氧元素的质量为![]() ,12.0g氧化铜中含氧元素的质量为
,12.0g氧化铜中含氧元素的质量为![]() ;
;
设三氧化硫的质量为x
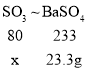
![]()
![]()
8g三氧化硫中含氧元素的质量为![]()
②和③共增重3.2g,这是二氧化硫的质量,其中含氧元素的质量为![]() ,
,![]() ,所以生成的气体中还有氧气,其质量为
,所以生成的气体中还有氧气,其质量为![]() ,故气体中还有O2。
,故气体中还有O2。
(5)该反应的化学方程式中,硫酸铜、氧化铜、二氧化硫、三氧化硫、氧气的化学计量数之比为![]() ,故化学方程式为
,故化学方程式为![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】老师为同学们提供了如图的实验装置:
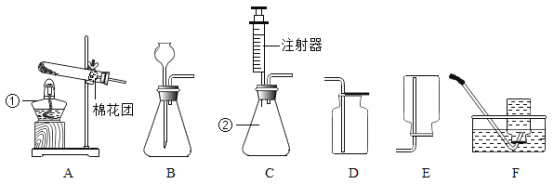
(1)写出仪器①②的名称:____________,____________。
(2)组装仪器时,将玻璃管插入胶皮管或带孔橡胶塞前,要先把玻璃管口_________,然后稍稍用力旋转,将其插入。
(3)①实验室可以选用稀盐酸和石灰石在装置B或C中制取二氧化碳,若选用C作发生装置,你认为装置C的优点是__________。
②也可以将注射器连接到装置B的导管口处,可用来__________。
(4)图G是实验室制取并检验CO2的“微型”装置,采用“微型”装置实验具有的优点是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某粗盐样品中含有少量MgSO4和CaCl2杂质,某化学兴趣小组欲除去其中的杂质,得到纯净的NaCl晶体,设计了如下图所示的实验方案。请回答下列问题:
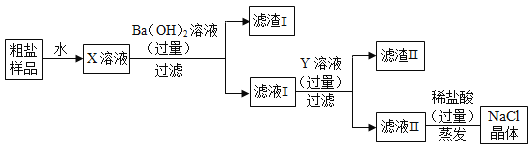
(1)写出X溶液中的杂质与Ba(OH)2溶液反应的化学方程式_____。
(2)滤液Ⅱ除氯化钠以外,还含有其他溶质成分,如何检验_____?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是X、Y两种固体物质的溶解度曲线图。请据图回答:
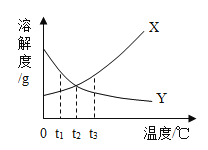
(1)t3°C时, 将澄清的饱和溶液X、Y降温到t2°C,有固休析出的是____________溶液。
(2)Y溶液的溶质可能是__________(填序号)。
ANaCl
BKNO3
CCa(OH)2
(3)t3°C时,保持温度不变,将X、Y饱和溶液蒸发一定量的水,则蒸发水后两溶液的溶质质量分数X____________Y (填“>”、“<”或“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙试管中各盛有10.0g水,向其中一支试管中加入3.0g Na2CO3粉末,另一支试管中加入3.0gNaCl粉末,按图1、2进行实验。下列说法正确的是
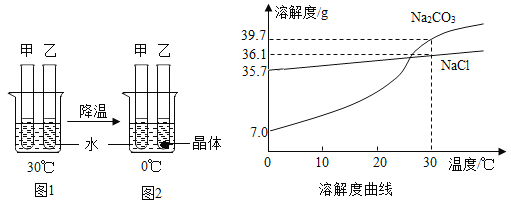
A.甲中加入的粉末是Na2CO3
B.0℃时,甲溶液溶质质量分数大于乙溶液
C.若将图1中的甲、乙溶液同时降温至t℃,一定都不会析出晶体
D.30℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】MgSO4和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是( )
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | |
溶解度 S/g | MgSO4 | 33.7 | 38.9 | 44.5 | 50.6 | 54.6 | 55.8 |
Na2SO4 | 19.5 | 40.8 | 48.8 | 47.5 | 45.3 | 44.8 | |

A. 甲为Na2SO4
B. t3℃应介于40℃~50℃之间
C. t4℃乙的饱和溶液,降温到t1℃的过程中,一直有晶体析出
D. b、c点乙的饱和溶液溶质质量分数相等,且大于a点甲的饱和溶液溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质A—E是初中化学常见的物质,如下图所示是物质A—E相互间的关系(“→”表示物质间存在的转化关系,“一”表示两端的物质能发生化学反应,微溶物质不考虑)。A、C、E中含有一种相同的元素,A是胃酸中的主要成分,A与B反应产生一种不溶于稀硝酸的白色沉淀,D是一种单质。请回答:
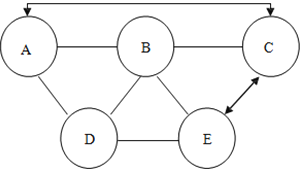
(1)A的化学式为________。
(2)A与D反应的实验现象是_________。
(3)B与C反应的化学方程式为________。
(4)E→C的化学方程式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】许多物质在常温时能与空气中的氧气、水蒸气、二氧化碳等物质发生反应而变质,下面我们对有关物质的变质情况进行探究。
探究一 生石灰常用作食品干燥剂,但是撕开包装袋后的生石灰常常粘接成块,其原因是__(写出任意一个反应的化学方程式)。
探究二 实验室有一瓶敞口放置的氢氧化钠溶液,对该溶液是否完全变质,小文同学进行如下探究:
实验步骤 | 实验现象 | 结 论 |
(1)取少量溶液于试管中,滴加足量氢氧化钡溶液。 | 有白色沉淀生成 | 氢氧化钠溶 液部分变质 |
(2)过滤,向滤液中加入____(填写一种盐溶液的化学式)。 | ______ |
(反思评价)经分析该实验存在明显的不足,我的改进建议是____。除去该氢氧化钠溶液中的杂质,发生反应的化学方程式为___。
(归纳整理)验证物质是否变质,其实质是要验证变质后的物质是否存在;验证物质是否完全变质,还要验证变质前的物质是否存在。
探究三 实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,智慧小组对一瓶久置的“碱石灰”变质情况作了如下探究。
(提出猜想)变质的碱石灰样品的主要成分可能含有氧化钙、氢氧化钠、氢氧化钙、碳酸钙和____(填化学式或名称均可,下同)。
(实验探究)小组讨论后设计如下实验进行探究:
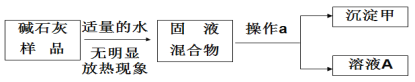
(思考分析)碱石灰样品中一定不含___,溶液A中溶质的组成可能有__种不同的组合。
(延伸探究)为了进一步验证碱石灰样品的成分,同学们继续设计实验:取少量溶液A于试管中,加入过量的氯化钡溶液和无色酚酞溶液,静置。小组同学对可能出现的现象、溶液A中溶质、碱石灰样品的成分进行如下
可能出现的实验现象 | A中溶质 | 碱石灰样品成分 |
有白色沉淀生成,上层清液为红色 | ___ | 一定含有碳酸钠和氢氧化钙。 |
有白色沉淀生成,上层清液为无色 | ___ | ___ |
(实践运用)由上述实验说明,实验室中“碱石灰”应密封保存。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com