
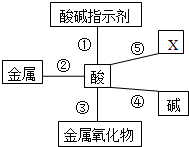
 构建知识网络能帮助我们理解知识间的内在联系.请分析如图酸的化学性质知识网络,完成下列问题:
构建知识网络能帮助我们理解知识间的内在联系.请分析如图酸的化学性质知识网络,完成下列问题:分析 根据酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、盐等反应)、金属的活动性等进行分析解答.
解答 解:(1)根据酸的化学性质,酸能与活泼金属、金属氧化物、碱、盐等反应,故①中可填写盐;
(2)若酸为稀硫酸,金属氧化物为氧化铁,反应③的化学方程式是:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)若酸为盐酸,金属为铜,反应②不能进行,理由是铜在氢后.
故答为:(1)盐;(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(3)不能,铜在氢后.
点评 本题难度不大,掌握酸的化学性质(能与酸碱指示剂、活泼金属、金属氧化物、碱、碳酸盐等反应)并能灵活运用是正确解答本题的关键.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 氮气充入食品中防腐,是利用氮气常温下化学性质稳定 | |
| B. | 氧气用于火箭发射,是利用氧气的可燃性 | |
| C. | 制作霓虹灯时充入稀有气体,是利用稀有气体通电能发出不同颜色的光 | |
| D. | 氦气可用来填充探空气球,是利用氦气的密度小 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 |
| 剪下一片变黑的铜片,放入盛有足量稀硫酸的试管中,微热 | 铜片表面黑色固体全部消失,露出红色的铜,溶液变蓝色. | 此黑色固体是CuO (填化学式) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 都具有可燃性可作燃料 | |
| B. | 在氧气中完全燃烧的产物相同 | |
| C. | 都具有还原性能够冶炼金属 | |
| D. | 与氧化铜发生的反应都属于置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验次数 | 1 | 2 | 3 |
| 加入稀硫酸的质量/g | 48 | 49 | 50 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | BaCl2+H2SO4═BaSO4↓+2HCl | B. | Mg(OH)2+2HCl=MgCl2+2H2O | ||
| C. | CuO+H2SO4=CuSO4+H2O | D. | SO2+2NaOH=Na2SO3+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com