
科目:初中化学 来源: 题型:选择题
| A. | 大于8mL | B. | 小于8mL | C. | 8mL | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分离木炭粉和氧化铜:将混合物在空气中充分灼烧 | |
| B. | 验证质量守恒定律:比较镁条燃烧前后固体的质量 | |
| C. | 除去铜粉中的铁粉:向混合物中加入足量的稀盐酸,充分反应后,过滤、洗涤、烘干 | |
| D. | 鉴别空气和二氧化碳:将带火星的木条分别伸入两瓶气体中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 |
| 剪下一片变黑的铜片,放入试管中,加入足量的稀硫酸 | 铜片表面的黑色物质全部消失,露出红色的铜,溶液变为蓝色. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 是一种化合物 | B. | 由碳、氢、氮三种元素组成 | ||
| C. | 所含碳元素的质量分数为40% | D. | 碳、氢、氮元素质量比2:8:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
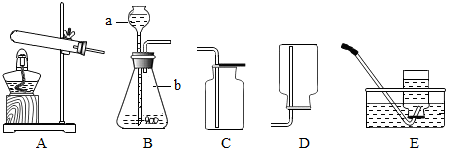
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
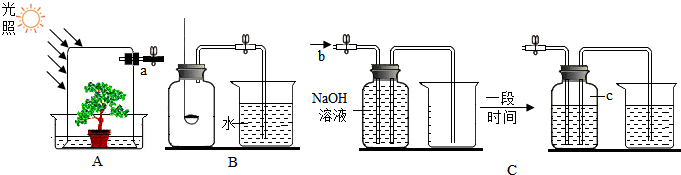
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com