
| A. | 烧杯中溶液质量不变 | B. | 烧杯中溶液质量增大 | ||
| C. | 烧杯中溶液颜色变浅 | D. | 烧杯中溶液颜色不变 |
分析 在金属活动性顺序中,镁比锌活泼,锌比银活泼,将一定量镁锌合金加入到硝酸银溶液中,镁先和硝酸银反应生成硝酸镁和银,如果镁不足,则锌再和硝酸银反应生成硝酸锌和银.镁比锌活泼,锌比铁活泼,可以分析滤渣加入到盛有硫酸亚铁溶液的烧杯中反应的情况.
解答 解:A、Mg+FeSO4═MgSO4+Fe
24 56
Zn+FeSO4═ZnSO4+Fe,
65 56
可见,镁和硫酸亚铁反应时溶液质量减小,锌和硫酸亚铁反应时溶液质量增大,烧杯中溶液质量不变,说明一定有镁参加反应,即滤渣中一定有镁,故错误;
B、镁和硫酸亚铁反应时溶液质量减小,锌和硫酸亚铁反应时溶液质量增大,烧杯中溶液质量增大,说明不能说明是否有镁参加反应,即滤渣中不一定没有镁,故错误;
C、硫酸镁溶液和硫酸锌溶液都是无色的,因此只要反应进行,溶液颜色变浅,因此烧杯中溶液颜色变浅,说明镁或锌与硫酸亚铁发生了反应,但是不能说明哪一种金属与硫酸亚铁反应,即不能说明滤渣中一定没有镁,故错误;
D、烧杯中溶液颜色不变,说明硫酸亚铁没有完全反应,镁、锌完全反应,即滤渣中一定没有镁,故正确.
故选:D.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.


科目:初中化学 来源: 题型:填空题
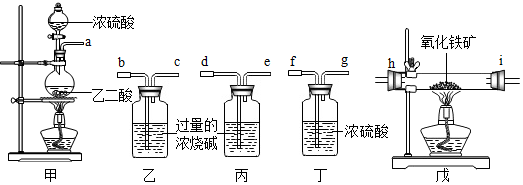
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
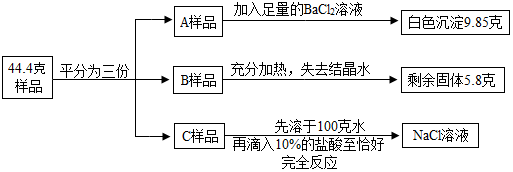
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 紫色石蕊 | B. | 无色酚酞 | C. | Na2CO3 | D. | AgNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 方案A | 方案B |
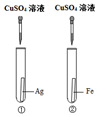 | 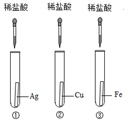 |
| (1)实验中发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu. (2)实验中观察到的现象是①中无明显变化,②中铁片表面覆盖一层红色物质,溶液由蓝色变成浅绿色. (3)该方案能(填“能”或“不能”)验证三种金属的活动性. | (1)实验中发生反应的化学方程式为Fe+2HCl=FeCl2+H2↑. (2)实验中观察到的现象是①②中均无明显变化,③中有气泡冒出,溶液由无色变成浅绿色. (3)该方案不能(填“能”或“不能”)验证三种金属的活动性. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
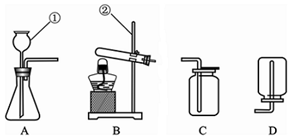
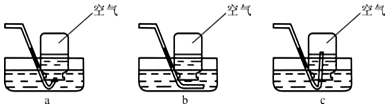
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
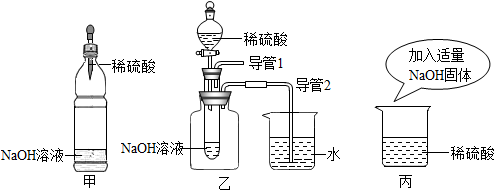
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com