
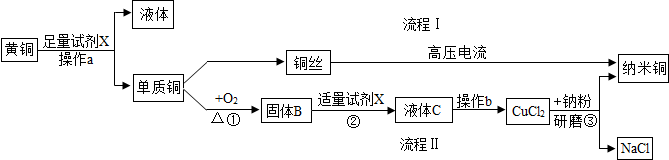
分析 根据黄铜的成分是铜和锌的混合物,要得到铜,需要除去锌,由于得到的是氯化铜,故加入的试剂X是盐酸,根据实验操作以及仪器的作用解答了根据反应物和生成物书写反应的化学方程式;据此解答.
解答 解:(1)根据实验流程中加入试剂X得到的是氯化铜溶液,故试剂X是稀盐酸,其化学式为HCl,固体B是铜与氧气反应生成的氧化铜,故填:HCl,CuO;
(2)操作a得到的是固体和溶液,故是过滤操作,所需要的玻璃棒作用是引流;操作b是蒸发,需用玻璃棒不断搅拌,其作用是使液体受热均匀,防止局部过热引起液体飞溅,故填:引流,使液体受热均匀;
(3)反应②是氧化铜和盐酸反应生成氯化铜和水,反应的化学方程式CuO+2HCl═CuCl2+H2O;反应③是金属钠与氯化铜的反应,属于置换反应故填;CuO+2HCl═CuCl2+H2O,置换;
(4)制备纳米铜流程中,流程Ⅰ没有产生新物质,是物理变化,故填:物理.
点评 本题考查的是常见的物质制备的知识,完成此题,可以依据已有的物质的性质结合题干提供的信息进行.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:选择题
| A. | 镁粉、氧化铜粉、木炭粉 | |
| B. | 氢氧化钠溶液、氢氧化钡溶液.氢氧化钾溶液 | |
| C. | 硫酸钠溶液、氯化钠溶液、氯化钡溶液 | |
| D. | 铝片、铁片、银片 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验目的 | 实验方法 | |
| A | 鉴别碳酸钠溶液和碳酸铵溶液 | 滴加石灰水 |
| B | 验证银、铜、铁的金属活动性 | 投入到足量FeSO4溶液中 |
| C | 验证质量守恒定律 | CuCl2溶液和稀硫酸混合 |
| D | 测定空气中O2含量 | 木炭燃烧 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 用科学方法认识和改造物质
用科学方法认识和改造物质查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com