
【题目】请用你具备的化学知识回答下面问题:
(1)收集二氧化碳不能用排水法原因是_____________________。
(2)夏天铁轨之间的缝隙变小的微观原因是_____________________。
(3)“洁厕灵”与“漂白精”不能混用,两者若混合易产生一种有毒气体X。 反应原理为:![]() ,则X的化学式为_____________________。
,则X的化学式为_____________________。
(4)暖气片表面常刷“银粉”(主要成分是铝)利用的是_____________________。
【答案】二氧化碳能溶于水,且与水反应 温度升高,铁原子间的间隔变大 ![]() 铝易于空气中氧气作用生成一层致密而坚固的氧化铝薄膜
铝易于空气中氧气作用生成一层致密而坚固的氧化铝薄膜
【解析】
铁轨是由铁原子构成的。
(1)二氧化碳能溶于水,且与水反应,不能用排水法收集,故收集二氧化碳不能用排水法原因是二氧化碳能溶于水,且与水反应。
(2)夏天铁轨之间的缝隙变小,是因为夏天气温高,温度升高,铁原子间的间隔变大。
(3)由质量守恒定律可知,反应前后,原子种类、数目均不变, 反应原理为![]() ,反应前有1个钠原子,3个氯原子,2个氢原子,1个氧原子,反应后有1个钠原子,1个氯原子,2个氢原子,1个氧原子,则每个X分子由2个氯原子构成,故物质X的化学式为
,反应前有1个钠原子,3个氯原子,2个氢原子,1个氧原子,反应后有1个钠原子,1个氯原子,2个氢原子,1个氧原子,则每个X分子由2个氯原子构成,故物质X的化学式为![]() 。
。
(4)暖气片表面常刷“银粉”(主要成分是铝),是因为铝易于空气中氧气作用生成一层致密而坚固的氧化铝薄膜,具有良好的抗腐蚀性。


科目:初中化学 来源: 题型:
【题目】实验技能训练中,小亮同学向氧化铜和稀硫酸充分反应后的废液中加入一定量的氢氧化钠溶液,发现无明显现象。小亮同学在老师的指导下对反应后的废液进行了实验:他分别取50g废液,并向其中逐渐加入等浓度的氢氧化钠溶液,三组实验的数据与其中一组的图象如下:
实验组数 | 第一组 | 第二组 | 第三组 |
加入氢氧化钠溶液质量/g | 50 | 100 | 80 |
产生沉淀的质量/g | 0.98 | 2.94 | 2.94 |
请根据以上信息回答下列问题:所得
(1)废液中的溶质有_____(填化学式)。
(2)计算废液中硫酸铜的溶质质量分数。_____(写出计算过程)
(3)若三组数据中,只有某一组加入的氢氧化钠溶液与废液恰好完全反应,则该实验为第_____组,下图中a的数值为_____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知反应前后有元素化合价改变的反应统称为氧化—还原反应,如图为反应类型的关系图,下列有关说法正确的是 ( )
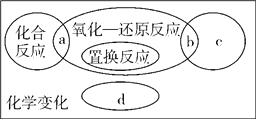
A. CO2+H2O=== H2CO3属于a处的反应
B. 2H2O![]() 2H2↑+O2↑属于氧化—还原反应
2H2↑+O2↑属于氧化—还原反应
C. c处反应后物质的质量一定减小,不符合质量守恒定律
D. 任何两种化合物之间发生反应都属于d
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】无水氯化钙在工业上有广泛的用途。以石灰石矿粉(含有SiO2、Fe2O3 、MgSO4等杂质)为原料,生产无水氯化钙的流程如图:
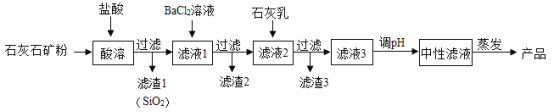
回答下列问题:
(1)从流程图中推知:SiO2具有的化学性质是________________。
(2)加入盐酸的主要作用是______________ ( 写化学方程式);
(3)滤渣3中除有Ca(OH)2外、还有_______________。(填化学式);
(4)产品中的杂质除极少量H2O外,最可能含的是______________ (填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组设计了一组实验,己知甲中盛有一定量的碳酸钠溶液,实验流程如图所示:下列说法正确的个数是
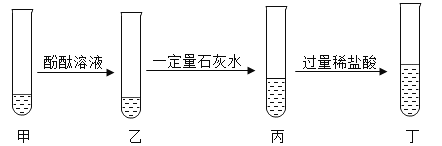
①乙中溶液为红色
②丙中溶液的溶质组成有2种可能情况
③丙中加入过量稀盐酸后,观察到的现象为有气泡产生,溶液由红色变为无色,白色沉淀消失
④丁中溶液的溶质除酚酞外,只有氯化钠、氯化氢
A.1
B.2
C.3
D.4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、 C、D是初中化学常见的四种不同类别的化合物,其中有一种物质中含有人体中含量最多的金属元素,C和D反应时能生成厨房中常用的一种调味品的主要成分。它们之间的反应和转化关系如图所示(“一”表示两物质能发生化学反应,“→”表示一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。回答下列问题。
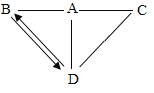
(1) B物质的名称_____。
(2)写出A和D反应的化学方程式_____。
(3)写出A和C的化学方程式_____。
(4)写出A物质的一种用途_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“喝酒不开车,开车不喝酒”。酒中含有乙醇(C2H6O),交通警察执法时让开车者对着便携式酒精检查仪吹气,便携式酒精检查仪内部发生反应的原理为:2K2Cr2O7(橙色) + 3C2H6O+8H2SO4 = 2Cr2(SO4)3(蓝绿色)+3C2H4O2+2K2SO4+11X,据该反应回答下列问题:
(1)如果司机饮了酒,交警观察到仪器内部药品发生反应的现象是______。
(2)便携式酒精检查仪中的铬(Cr)元素在检查前后的质量____(填“增加”、“减少”、“不变”)。
(3)该反应生成物中X的化学式为_____。
(4)Cr元素的化合价在反应前后的变化是______(填由多少价变到多少价)。
(5)乙醇也是一种燃料,在空气中完全燃烧生成水和二氧化碳。乙醇在空气中完全燃烧的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学对“锌与硫酸反应速率的影响因素”进行探究,并利用如图装置收集产生的氢气。
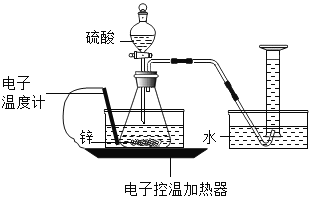
(查阅资料)
圆粒状锌的直径通常为 3-4 毫米,粉末状锌的直径通常为 0.3-0.5 毫米。
(进行实验)
实验 1:在不同温度下,进行锌与硫酸反应的实验。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
1-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
1-2 | 30 | 20 | 10% | 圆粒状 | 1 | 134 |
1-3 | 40 | 20 | 10% | 圆粒状 | 1 | 107 |
实验 2:在相同温度下,继续进行锌与硫酸反应速率的影响因素的探究。
编号 | 温度/℃ | 硫酸体积/ mL | 硫酸溶质质量分数 | 锌的形状 | 锌的质量 /g | 收集30mL氢气所用的时间/s |
2-1 | 20 | 20 | 10% | 圆粒状 | 1 | 170 |
2-2 | 20 | 20 | 10% | 粉末状 | 1 | 47 |
2-3 | 20 | 20 | 20% | 圆粒状 | 1 | 88 |
2-4 | 20 | 20 | 20% | 粉末状 | 1 | 26 |
(解释与结论)
(1)锌与硫酸反应的化学方程式为_____ 。
(2)能用排水法收集氢气的原因是氢气_____(填“易”或“难”)溶于水。
(3)实验 1 的目的是_____。
(4)实验 2 中,欲得出“其他条件相同时,硫酸的溶质质量分数越大,锌与硫酸反应的速率越快”的结论,需要对比的实验_____(填编号)。
(5)实验 2 中,通过对比 2-1 和 2-2,得出的结论是_____。
(反思与评价)
(6)实验室制取氢气时,通常使用锌粒而不用锌粉的原因为_____。
(7)实验室中若使用 6.5g 锌粒制取氢气,理论上制得氢气的质量为_____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com