
| A. | 25% | B. | 50% | C. | 60% | D. | 75% |
分析 可以假设出氯酸钾的质量,然后根据固体中钾元素与氧元素的质量比可以计算已分解的氯酸钾占原氯酸钾的质量分数.
解答 解:设氯酸钾的质量是245g,
245g氯酸钾中钾元素的质量为:245g×$\frac{39}{122.5}$×100%=78g,氧元素的质量为:245g×$\frac{48}{122.5}$×100%=96g,
即245g氯酸钾中钾元素和氧元素的质量比为:78g:96g=78:96,
因为蒸干后的固体中钾元素与氧元素的质量比为:39:24=78:48,所以反应中有48g氧气生成,即氧元素损失了50%,说明氯酸钾分解了50%.
故选:B.
点评 因为反应的化学方程式中,2KClO3的相对分子质量和是245,因此设氯酸钾的质量是245g计算起来比较容易,同时是求氯酸钾的分解率,与氯酸钾的质量大小无关,要注意理解.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 溶液都是无色、均一、稳定的液体 | |
| B. | 在水中加入氯化钠可以增强水的导电性 | |
| C. | 用汽油清洗衣服上的油漆发生乳化现象 | |
| D. | 用高锰酸钾制取氧气实验,收集完氧气后先移导管后移酒精灯 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
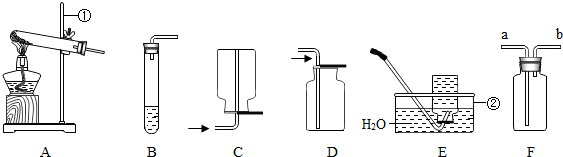
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
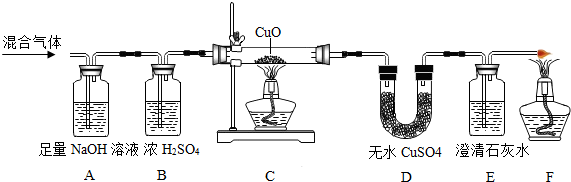
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com