
 ��ʵ��������dz��ô���ʯ�����ᷴӦ��ȡ������̼��ij����ʯ��Ҫ�ɷ�ΪCaCO3���������������������ص����ϣ���֪̼���������ĸ��ֽⷴӦ���Է����У��ڳ����£����Ũ�Ⱦ�Ϊa%��������Һ��pH��С���������
��ʵ��������dz��ô���ʯ�����ᷴӦ��ȡ������̼��ij����ʯ��Ҫ�ɷ�ΪCaCO3���������������������ص����ϣ���֪̼���������ĸ��ֽⷴӦ���Է����У��ڳ����£����Ũ�Ⱦ�Ϊa%��������Һ��pH��С���������| ���� | H2SO4 | HCl | H2S | H2CO3 |
| pH | �������������������������� | |||
| ���� | H2SO4 | HCl | H2S | H2CO3 |
| pH | �������������������������� | |||


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���μ���������Һ |
| B���������� |
| C���μӳ���ʯ��ˮ |
| D���μӷ�̪��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ȼ���������ں������ |
| B������ȼ������ȼ�գ�����ˮҲ�п�ȼ�� |
| C������ȼ����ȼ�պ��������κβ�������� |
| D������ȼ����������Ȼ����ȴ��õ��Ĺ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
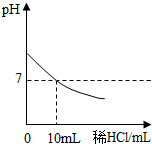 ��һ����NaOH��Һ�У��μ�ϡHCl�����������������ҺpH�ı仯��ͼ��ʾ��
��һ����NaOH��Һ�У��μ�ϡHCl�����������������ҺpH�ı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�鲽�� | ʵ������ | ʵ����� |
| ��1��ȡ�����ù������Թ��У���ˮ�ܽ⣬����Һ�еμӹ����Ȼ�����Һ���������� | �а�ɫ���������� | ˵��ԭ������һ������ |
| ��2��ȡ��1���Թ��е��ϲ���Һ���μӷ�̪��Һ�� | ��Һ���ɫ�� | ˵��ԭ������һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ʵ����� | ʵ������ | ���� |
| ����һ | ȡ������Һ���Թ��У�����Һ�в���һ��ͭ˿ | ����ٳ��� | |
| ����ڳ��� | |||
| ������ | ����ٳ��� | ||
| ����ڳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| NH3 | N2 | NO | NO2 | |
| �ɫ | ��ɫ | ��ɫ | ��ɫ | ����ɫ |
| �ܽ��� | ��������ˮ | ������ˮ | ������ˮ | ������ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ʒ�� | �ƶ���-D | ��˼��-D | ������ | ������� |
| ��Ҫ�������� | ̼��� | ̼��� | ̼��� | ������� |
| ��Ԫ�غ�����mg/Ƭ�� | 600 | 500 | 250 | 168 |
| ������Ƭ/ƿ�� | 30 | 20 | 30 | 30 |
| �۸�Ԫ/ƿ�� | 27.00 | 23.10 | 30.00 | 25.20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
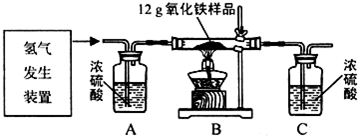 ijͬѧΪ�ⶨ12g�����ʵ���������Ʒ������������������������ϡ�����п����ȡ�������������ͼ��ʾ��װ�ã������йص�ʵ��̽�������ʲ��μӷ�Ӧ���ٶ�ÿ������ȫ��Ӧ�����գ��ҷ�ӦǰCװ������Ϊ284.2g����Ӧ��Cװ������Ϊ286.9g�����������Ʒ����������������������д�����㲽�裬��������ȷ��0��l%��
ijͬѧΪ�ⶨ12g�����ʵ���������Ʒ������������������������ϡ�����п����ȡ�������������ͼ��ʾ��װ�ã������йص�ʵ��̽�������ʲ��μӷ�Ӧ���ٶ�ÿ������ȫ��Ӧ�����գ��ҷ�ӦǰCװ������Ϊ284.2g����Ӧ��Cװ������Ϊ286.9g�����������Ʒ����������������������д�����㲽�裬��������ȷ��0��l%���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com