



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| Ń”Ļī | ŹµŃéÄæµÄ | ·½·ØŅ» | ·½·Ø¶ž |
| A | Ö¤Ć÷¼ÆĘųĘæÖŠŹ¢×°¶žŃõ»ÆĢ¼ĘųĢå | ÉģČėČ¼×ŵÄľĢõ | µ¹Čė³ĪĒåŹÆ»ŅĖ® |
| B | ¼ģŃéĀČ»ÆÄĘÖŠŗ¬ÓŠĒāŃõ»ÆÄĘ | µĪ¼Ó·ÓĢŖČÜŅŗ | ¼ÓČėŃĪĖį |
| C | ³żČ„ĀČ»ÆÄĘČÜŅŗÖŠµÄĢ¼ĖįÄĘ | ¼ÓČėŹŹĮæŃĪĖį | ¼ÓČėŹŹĮæ³ĪĒåŹÆ»ŅĖ®£¬¹żĀĖ |
| D | ¼ģŃéCOÖŠŗ¬ÓŠÉŁĮæµÄCO2 | ĶØČė³ĪĒåŹÆ»ŅĖ®³ĪĒåŹÆ»ŅĖ® | ĶØČė×ĻÉ«ŹÆČļŹŌŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
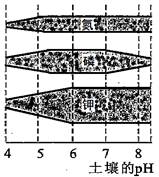
| A£®ĶĮČĄĖįŠŌŌ½Ē棬ֲĪļ¶ŌČżÖÖŌŖĖŲµÄĪüŹÕĀŹŌ½øß |
| B£®ĶĮČĄ¼īŠŌŌ½Ē棬ֲĪļ¶ŌĮ×ŌŖĖŲµÄĪüŹÕĀŹŌ½øß |
| C£®ĶĮČĄ pH="8" Ź±£¬Ö²Īļ¶ŌČżÖÖŌŖĖŲĪüŹÕĀŹ×īøߵďĒ¼Ų |
| D£®Ö²ĪļĶ¬Ź±ĪüŹÕČżÖÖŌŖĖŲµÄĶĮČĄ pH ×ī¼Ń·¶Ī§£ŗ5”«6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®·Ö×ÓŹĒ¹¹³ÉĪļÖŹµÄĪ¢Į££¬ĪļÖŹ¶¼ŹĒÓÉ·Ö×Ó¹¹³ÉµÄ |
| B£®Ńõ»ÆĪļŅ»¶Øŗ¬ŃõŌŖĖŲ£¬ŗ¬ŃõŌŖĖŲµÄĪļÖŹŅ»¶ØŹĒŃõ»ÆĪļ |
| C£®ÖŠŗĶ·“Ӧɜ³ÉŃĪŗĶĖ®£¬Éś³ÉŃĪŗĶĖ®µÄ·“Ó¦Ņ»¶ØŹĒÖŠŗĶ·“Ó¦ |
| D£®¼īŠŌ½ĻĒæµÄČÜŅŗÄÜŹ¹·ÓĢŖČÜŅŗ±äŗģ£¬ÄÜŹ¹·ÓĢŖČÜŅŗ±äŗģµÄČÜŅŗŅ»¶Ø³Ź¼īŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| ŅõĄė×ÓŃōĄė×Ó | OH”Ŗ | Cl”Ŗ |
| Ca2+ | ¢Ł | ČÜ |
| Zn2+ | ²» | ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®O2 | B£®SO2 | C£®H2 | D£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| ĪļÖŹ | CaO | CaCO3 | Ca(OH)2 | NaOH |
| ŹŠ³”²Īæ¼¼Ū£ØŌŖ£Ækg £© | 3.5 | 2.5 | 2.8 | 11.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®CO2 | B£®Na2CO3 | C£®HCl | D£®CuSO4 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com