
分析 (1)根据日常生活中降低水的硬度的方法进行分析;
(2)根据较为清洁的燃料是天然气,天然气的主要成分是甲烷进行分析;
(3)根据化学变化前后原子的种类、数目不变进行分析.
解答 解:(1)硬水中含有较多的可溶性的Ca2+和Mg2+,沉淀只能除去水中颗粒较大的不溶性物质;过滤是除去水中的不溶于水等杂质,没有软化水;蒸馏可以使水中的可溶性钙镁化合物分解,而降低水的硬度;
(2)化石能源中较为清洁的燃料是天然气,天然气的主要成分是甲烷,甲烷是由碳、氢两种元素组成的;
活性炭具有吸附作用,能够吸附色素和异味,在饮水机里,用活性炭来除去水中异味;
(3)由反应的化学方程式C3H8O+4O2$\frac{\underline{\;点燃\;}}{\;}$4H2O+2CO2+X,反应前后各原子的个数依次为
反应前 反应后
C原子 3 2
H原子 8 8
O原子 9 8
根据化学变化前后原子的种类、数目不变,可判断物质X的分子由1个C原子和1个O原子构成,则物质X的化学式可表示为CO;
故答案为:(1)蒸馏法;(2)碳、氢;(3)CO.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.


 优百分课时互动系列答案
优百分课时互动系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 燃烧需要可燃物接触氧气,所以可燃物接触氧气就一定能燃烧 | |
| B. | 用洗洁剂洗去油污是利用了乳化作用,用汽油洗去油污也是利用了乳化作用 | |
| C. | 溶液具有均一、稳定的特征,所以均一、稳定的液体一定是溶液 | |
| D. | 铁与稀硫酸反应后溶液质量增大,锌与稀硫酸反应后溶液质量也增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
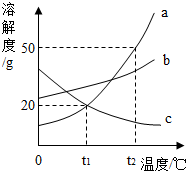 a、b、c三种固体物质的溶解度曲线如图所示,请回答:
a、b、c三种固体物质的溶解度曲线如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
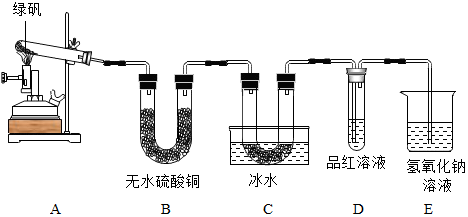
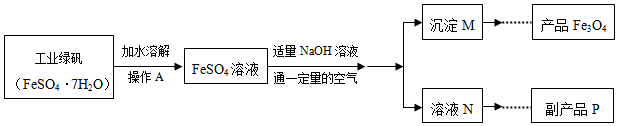
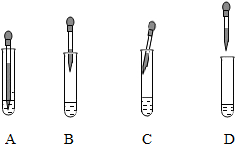

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
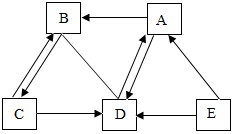 A、B、C、D、E是初中化学常见的物质.C为单质;生活中B 和D都可用来灭火; E广泛用于玻璃、造纸、纺织、洗涤剂的生产.它们之间的一部分关系如图所示,(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.部分反应物或生成物已略去)
A、B、C、D、E是初中化学常见的物质.C为单质;生活中B 和D都可用来灭火; E广泛用于玻璃、造纸、纺织、洗涤剂的生产.它们之间的一部分关系如图所示,(图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系.部分反应物或生成物已略去)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com