
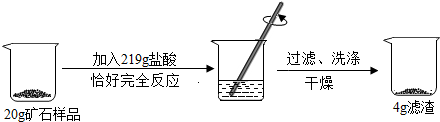
分析 (1)根据赤铁矿石中的杂质既不溶于水也不和酸反应,则矿石反应后固体减少的质量为矿石中氧化铁的质量,然后计算氧化铁的质量分数;
(2)根据氧化铁与一氧化碳反应的化学方程式,由反应消耗氧化铁的质量计算出参加反应的盐酸的质量分数.
解答 解:(1)赤铁矿石中氧化铁的质量分数为:$\frac{20g-4g}{20g}$×100%=80%;
(2)设参加反应的盐酸的质量为x
6HCl+Fe2O3=2FeCl3+3H2O
219 160
x 16g
$\frac{219}{x}$=$\frac{160}{16g}$
x=21.9g
盐酸的质量分数为:$\frac{21.9g}{219g}$×100%=10%.
故答案为:(1)80%;
(2)10%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.


科目:初中化学 来源: 题型:解答题
 某学习小组用如图所示装置进行镁条(足量)在空气中燃烧的实验.当燃烧停止、冷却后打开弹簧夹.进入集气瓶中水的体积约占瓶内原液面以上容积的70%.请根据实验回答下列问题.
某学习小组用如图所示装置进行镁条(足量)在空气中燃烧的实验.当燃烧停止、冷却后打开弹簧夹.进入集气瓶中水的体积约占瓶内原液面以上容积的70%.请根据实验回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图,某化学兴趣小组设计了一组“吹气球”实验.
如图,某化学兴趣小组设计了一组“吹气球”实验.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
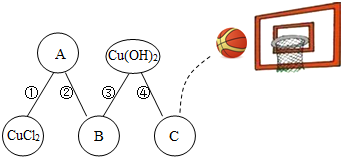 物质王国举行一场趣味篮球赛.某队由铁、二氧化碳、稀盐酸、氢氧化钙、氯化铜五名“队员”组成.比赛中,由“氯化铜队员”发球,“队员”间传接球,最后由C位置“队员”投篮进球完成有效进攻.传接球“队员”间必须能相互反应,场上“队员”位置及传球路线如图.
物质王国举行一场趣味篮球赛.某队由铁、二氧化碳、稀盐酸、氢氧化钙、氯化铜五名“队员”组成.比赛中,由“氯化铜队员”发球,“队员”间传接球,最后由C位置“队员”投篮进球完成有效进攻.传接球“队员”间必须能相互反应,场上“队员”位置及传球路线如图.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 缺铁易引起贫血 | B. | 老年人缺钙易患骨质疏松症 | ||
| C. | 缺碘会引起甲状腺肿大 | D. | 青少年预防佝偻病,应适量补锌 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com