
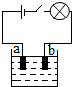
 小李同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如表:
小李同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按如图所示的装置进行实验,实验结果记录如表:| 物质 导电性 状态 | 食盐NaCl | 硝酸钾KNO3 | 蔗糖C12H22O18 | 氢氧化钠NaOH | 硫酸铜CuSO4 |
| 固态 | × | × | × | × | × |
| 熔化状态 | √ | √ | × | √ | √ |
| 水溶液 | √ | √ | × | √ | √ |
分析 根据电解质的概念、能量的转化以及硫酸铜和氢氧化钡的反应进行分析解答即可
解答 解:(1)根据表格提供的数据可以看出,蔗糖不具有导电性,因此不是电解质;
(2)电解质溶液在导电的同时,在电极a、电极b上都会有新的物质生成.说明能将电能转化为化学能;电极a、b应具有的性质是在熔化或水溶液中能导电;
(3)由于氯离子带负电.当闭合开关后,氯离子能向正极移动;
(4)硫酸铜与氢氧化钡反应生成氢氧化铜沉淀和硫酸钡沉淀,故开始时溶质减少则灯泡逐渐变暗,当恰好完全反应,不含有溶质,故灯泡熄灭,再继续加入氢氧化钡,又含有电解质,故逐渐变亮,所以灯泡的亮度先变暗直至熄灭后逐渐变亮.
故答案为:(1)蔗糖;(2)化学、在熔化或水溶液中能导电;(3)Cl-;(4)先变暗直至熄灭后逐渐变亮.
点评 本题考查的是实验的知识,完成此题,可以依据题干提供的信息结合物质的性质进行.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 同种元素的原子具有相同的质子数,所以具有相同质子数的两种粒子一定是同种元素 | |
| B. | 由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成 | |
| C. | 单质都是由一种元素组成的,所以含有一种元素组成的物质一定是单质 | |
| D. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
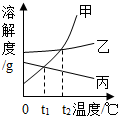 如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答
如图为甲、乙、丙三种固体物质在水中的溶解度曲线,请回答查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com