
| A. | 酶只能在细胞内起作用 | |
| B. | 一种酶只能催化某一种或某一类化学反应 | |
| C. | 酶的催化作用受到温度、pH 的影响 | |
| D. | 酶是生物体细胞制造的一种蛋白质 |
分析 酶是生物体内活细胞产生的生物催化剂,在体内的化学反应中能够加快反应速度;绝大多数酶的化学本质是蛋白质.具有催化效率高、专一性强、作用条件温和等特点.
解答 解:A、有些酶在细胞内起催化作用,有些酶在细胞外也能起催化作用,例如所有的消化酶都是在消化道内起催化作用的;故符合题意.
B、一种酶只能催化一种或一类化学反应,例如唾液淀粉酶只能催化淀粉分解为麦芽糖,对食物中的其它营养物质的分解就没有作用,这就是酶的专一性;故不符合题意.
C、由于大多数酶是蛋白质,因而会被高温、强酸、强碱等破坏而失去活性,因此酶的催化作用受温度、pH值的影响;故不符合题意.
D、酶是生物活细胞产生的生物催化剂,是一类特殊的蛋白质;故不符合题意.
故选:A
点评 酶是一种生物催化剂.生物体内含有千百种酶,它们支配着生物的新陈代谢、营养和能量转换等许多催化过程,与生命过程关系密切的反应大多是酶催化反应.但是酶不一定只在细胞内起催化作用.


科目:初中化学 来源: 题型:解答题
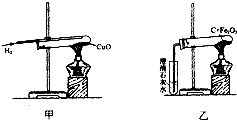
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu+H2SO4═CuSO4+H2↑ | B. | Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | 2Al+6HCl═2AlCl3+3H2↑ | D. | CaCl2+2KNO3═Ca(NO3)2+2KCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
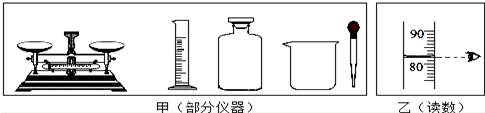
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某品牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.
某品牌变色眼镜的镜片在强光下会变成暗棕色,当光线变暗时,镜片几乎变成无色透明.原来,变色眼镜是在普通镜片中加入了适量的溴化银和氧化铜的微晶粒.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
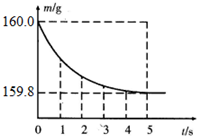 小李要测定某Cu-Zn合金中铜的质量分数,做了如下实验.
小李要测定某Cu-Zn合金中铜的质量分数,做了如下实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com