
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 带火星的木条复燃. | 质量不变 | 过氧化氢溶液中: 有气泡冒出 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
分析 【猜想】根据催化剂的含义进行解答;
【实验】(1)根据氧化铁对过氧化氢的分解有催化作用回答;
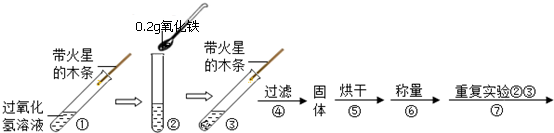
(2)根据步骤①的目的是检验过氧化氢溶液是否会自发的分解放出氧气进行解答;
(3)根据过氧化氢分解生成水和氧气进行解答;
(4)根据步骤⑦重复实验②、③的目的是判断氧化铁在过氧化氢分解前后化学性质是否改变进行解答;
【继续探究】根据科学探究的环节探究催化剂表面积大小、使用量等影响化学反应速率.
解答 解:【猜想】Ⅲ氧化铁是反应的催化剂,反应前后质量和化学性质均不变;故填:质量和化学性质均不变;
【实验】(1)氧化铁对过氧化氢的分解有催化作用,质量反应前后不变;故填:质量不变;有气泡冒出;
(2)步骤①的目的是检验过氧化氢溶液是否会自发的分解放出氧气;故填:检验过氧化氢溶液是否会自发的分解放出氧气;
(3)过氧化氢分解生成水和氧气,文字表达式为:过氧化氢$\stackrel{氧化铁}{→}$水+氧气;故填:过氧化氢$\stackrel{氧化铁}{→}$水+氧气;
(4)步骤⑦重复实验②、③的目的是判断氧化铁在过氧化氢分解前后化学性质是否改变;故填:判断氧化铁在过氧化氢分解前后化学性质是否改变;
【继续探究】科学探究的环节探究催化剂表面积大小、使用量等影响化学反应速率.
所以实验方案:猜想1:催化剂表面积大小影响化学反应速率.
实验方法:用两支试管各盛放5mL5%的过氧化氢溶液,分别加入0.2g粉末状和颗粒状的氧化铁,观察气体产生的速率.
猜想2:催化剂的使用量影响化学反应速率.
实验方法:用两支试管各盛放5mL5%的过氧化氢溶液,分别加入0.2g和0.5g颗粒大小相同的氧化铁,观察气体产生的速率.
故答案为::猜想1:催化剂表面积大小影响化学反应速率.
实验方法:用两支试管各盛放5mL5%的过氧化氢溶液,分别加入0.2g粉末状和颗粒状的氧化铁,观察气体产生的速率.
猜想2:催化剂的使用量影响化学反应速率.
实验方法:用两支试管各盛放5mL5%的过氧化氢溶液,分别加入0.2g和0.5g颗粒大小相同的氧化铁,观察气体产生的速率.
点评 催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在通常情况下,氧气是一种无色、无味的气体 | |
| B. | 氧气不溶于水 | |
| C. | 氧气的密度比空气的大 | |
| D. | 氧气是一种化学性质比较活沷的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com