
| A�� | �������ΪZn��Al��w������0.2g | |
| B�� | �������ΪZn��Fe��w��������0.2g | |
| C�� | �������ΪZn��Cu��w��0.2g����û������п����������Ϊ50% | |
| D�� | �������ΪZn��Mg��������ϡ������������������һ������10% |
���� ������Բ�ȡ���跨�ͼ�ֵ�����з���˼����Ҳ�����ȼ�������һ�ɷ����������������ҳ��������ݣ��������������֮�䣮
��� �⣺���ȼ������Ǵ�����п����6.5gп��Ӧ�������Լ�������������
Zn+H2SO4=ZnSO4+H2��
65 98 2
6.5g 9.8g 0.2g
�������Ľ���������������ȫ��Ӧ�õ������ɶൽ�ٵ�˳��Ϊ��þ������п�أ��ɼ�þ������������пǿ�������������Ϊп������õ�������һ������0.2g������A�����������Ϊп��������õ�����һ������0.2g������B��ȷ��������пͭ����õ�������һ��С��0.2g������C����
����6.5g�Ǵ�����þ�����Ӧ��������ϵΪ
Mg+H2SO4=MgSO4+H2��
24 98 2
6.5g 26.5g 0.54g
�ɼ�ϡ��������������Ӧ�ý���9.8%��26.5%������һ������10%��˵���Ǵ���ģ�����D����
��ѡ��B��
���� ���ݻ�ѧ����ʽ����ʱ����һҪ��ȷ��д��ѧ����ʽ���ڶ�Ҫʹ����ȷ�����ݣ������������Ҫ�������������Ľ���������������ȫ��Ӧ�õ������ɶൽ�ٵ�˳��Ϊ��þ������п�أ�������ۿ��Լ�ס���ڽ�����ͼ���ⳣ�ã��ڽ���������ɷַ�����Ҳ���ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
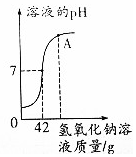 �ձ�����100g���ʵ���������Ϊ9.8%��ϡ���ᣬ���ձ�����������������Һ���ձ�����Һ��pH���������������Һ�����ı仯��ϵ��ͼ��ʾ��
�ձ�����100g���ʵ���������Ϊ9.8%��ϡ���ᣬ���ձ�����������������Һ���ձ�����Һ��pH���������������Һ�����ı仯��ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ��������������ǰС | |
| B�� | �������Һ��������������ǰ��� | |
| C�� | ����������Һ������������ش� | |
| D�� | �������Һ�������������������ƴ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2SO4��Na2O��KCl��CO | B�� | Mg��OH��2��CuSO4��HCl��CO2 | ||
| C�� | KOH��HNO3��NaCl��SO3 | D�� | HCl��NaOH��NaCl��P2O5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H5OH��NaCl ��Һ������ζ�� | B�� | NaOH��Һ��ϡH2SO4��Һ����̪��Һ�� | ||
| C�� | Ca��OH��2��Һ��NaOH��Һ��ϡ���ᣩ | D�� | KMnO4 ��KClO3 ���۲���ɫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com