
| ①酸与指示剂作用 | 酸溶液能使紫色石蕊 溶液变红色 | 酸溶液不能使无色酚酞 溶液变色 |
| ②酸与活泼金属作用 | Fe+2HCl=FeCl2+H2↑ | Fe+H2SO4=FeSO4+H2↑ |
| ③酸与某些金属氧化物作用 | Fe2O3+HCl=FeCl3+H2O | … |
| ④… | ||
分析 (1)配平化学方程式要遵循质量守恒定律,即等号两边元素的原子个数相等;
(2)①推广使用中国铁锅,使用铁锅炒菜时能补充人体需要的微量元素;该反应原理利用了酸与活泼金属反应;②食醋在厨房中的妙用还很多,如用来除水垢、除铁锈等.
解答 解:(1)配平后的化学方程式:Fe2O3+6HCl=2FeCl3+3H2O;
(2)胃酸的成分是HCl;推广使用中国铁锅,使用铁锅炒菜时能补充人体需要的微量元素铁元素;该反应的原理是利用了酸的化学性质酸与活泼金属反应,即题表中②.
故答案为:
(1)Fe2O3+6HCl=2FeCl3+3H2O;
(2)HCl;铁;②.
点评 此题主要考查酸的化学性质及具有相似化学性质的原因,金属的化学性质,化学方程式的配平,食醋在厨房中的妙用等知识点,题型设计新颖,考查了学生结合实际生活解决化学问题的能力.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
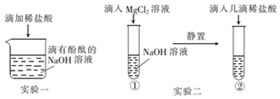 实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:
实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ⑤②④③① |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 强腐蚀性,阴冷,密封贮藏 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com