
| PH值 | 0-5.5 | 5.5-8 | 8-14 |
| 存在形式 | Al3+ | Al(OH)3 | AlO2- |
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
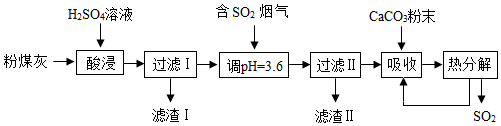
(1)酸浸时使用过量的稀硫酸的目的是使氧化铝完全反应,是氧化铝和硫酸反应生成硫酸铝和水,对应的化学方程式为 Al2O3+3H2SO4=Al2(SO4)3+3H2O;滤渣Ⅰ的主要成分为 SiO2(填化学式).
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6-2x.这个过程碳酸钙和硫酸反应生成了硫酸钙和水,而硫酸钙是微溶的,所以滤渣Ⅱ的主要成分为 CaSO4;若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是铝离子转化为氢氧化铝而沉淀.
(3)由于信息提示“②+4价的硫元素具有还原性,易被氧气等物质氧化为+6硫元素”,所以上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是被氧气氧化为+6价成为稳定的硫酸而不再释放出二氧化硫;与吸收SO2前的溶液相比,热分解前是弱酸性的亚硫酸溶液,而热分解后是强酸硫酸,酸性越强,pH越小,所以热分解后循环利用的溶液的pH将减小.
故答案为:
(1)使氧化铝完全反应,Al2O3+3H2SO4=Al2(SO4)3+3H2O; SiO2.
(2)CaSO4; 铝离子转化为氢氧化铝而沉淀.
(3)被氧气氧化为+6价成为硫酸; 减小.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
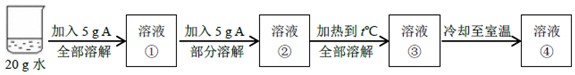
| A. | 在室温下,溶液①为饱和溶液 | B. | 在t℃时,A的溶解度一定为50克 | ||
| C. | 溶液②和溶液④的溶质质量分数相同 | D. | 溶液③和溶液④的溶液质量相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 排水法收集氧气,要等导管口气泡均匀连续冒出时再开始收集 | |
| B. | 保持空气化学性质的最小粒子是空气分子 | |
| C. | 检验氢氧化钠与氯化铵反应生成的气体可用湿润的蓝色石蕊试纸 | |
| D. | 不同种元素最本质的区别是中子数不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
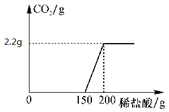 老师拿出一瓶没有瓶盖的氢氧化钠固体取出50g样品实验如图,请同学们进行分析:(如图所示)
老师拿出一瓶没有瓶盖的氢氧化钠固体取出50g样品实验如图,请同学们进行分析:(如图所示)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| A. | 氯化铵的溶解度随温度升高而增大 | |
| B. | 10℃时,100 g水中最多溶解33.3g氯化铵固体 | |
| C. | 30℃时,氯化铵饱和溶液的溶质质量分数为41.4% | |
| D. | 氯化铵的饱和溶液中还能溶解其他物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用燃着的酒精灯引燃另一盏酒精灯 | |
| B. | 在点燃氢气之前先检验氢气的纯度 | |
| C. | 与滴瓶配套的胶头滴管使用完毕,清洗后放回原瓶 | |
| D. | 稀释浓硫酸时,将水沿玻璃棒慢慢注入浓硫酸中,并不断搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
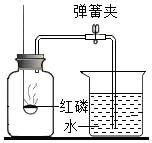 如图是用燃磷法测定“空气中氧气含量”的实验,下列说法正确的是( )
如图是用燃磷法测定“空气中氧气含量”的实验,下列说法正确的是( )| A. | 装置中的红磷可以用铁丝来代替 | |
| B. | 待红磷熄灭并冷却后,打开弹簧夹,再观察现象 | |
| C. | 红磷在空气中燃烧产生大量的白雾 | |
| D. | 实验测定氧气的质量约占空气总质量的$\frac{1}{5}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com