
【题目】某小组对H2O2溶液制取氧气进行了如下探究:
【探究一】:探究不同催化剂对H2O2分解快慢的影响
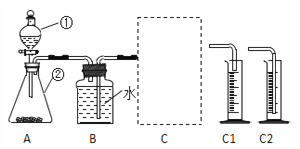
该小组采用了如下图所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液浓度均为10%20mL,在C框中连接导管和量筒,并测量收集到50mL水时的某项数据,经计算后的数据如下表:
催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
(1)检查A装置气密性的方法是:用弹簧夹夹住A装置右侧导气管,打开①的两个活塞,向其中加水,若___________,则气密性良好。
(2)C框内选用C1或C2装置,对该探究实验结论有无影响______。
(3)从实验数据可知:相同条件下表中催化剂的催化效果由强到弱依次为________。
(4)该探究实验中,需要测定的数据是____________。
(5)当量筒中收集到50mL水时,双氧水分解出的氧气体积______50mL(填“大于”、“等于”、“小于”)。
【探究二】:探究H2O2溶液浓度对分解速率的影响
如图:在250mL三颈瓶中,加入MnO2均为0.5g,在恒压漏斗中加入不同浓度的H2O2溶液各20mL分别进行实验。并用温度传感器测量并绘制出瓶内温度与时间关系图。如下图所示。
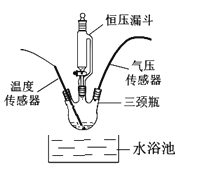
再将该装置的三颈瓶浸入水浴池中(该池可使瓶内的溶液温度恒定在20℃),用上述实验中相同量的各物质重复上述实
验,用气压传感器测量并绘制出瓶内气压与时间关系图。如下图所示。
(6)实验中,恒压漏斗的作用是__________。
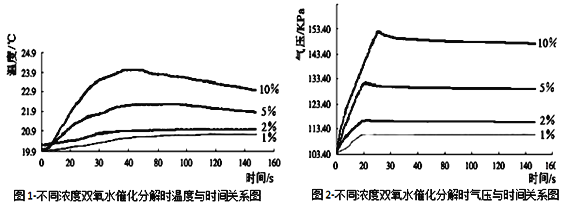
(7)由图1知道:H2O2溶液分解时会_________热量(填“放出”或“吸收”)。
(8)由图2知道: H2O2溶液浓度越高,其分解反应速率越______(填“快”或“慢”),以10%H2O2溶液为例,20S后三颈瓶内气压约由高缓慢降低的原因是_________。
(9)影响H2O2溶液分解速率的因素,除了催化剂的种类、H2O2溶液浓度外,还可能有的因素如:__________(请写出一种)。
【答案】 一段时间后,漏斗中的水不滴下(或漏斗下管口有水柱) 无 活性炭>CuO>MnO2 收集50mL氧气所需的时间 小于 使恒压漏斗与三颈瓶内气压相等,便于H2O2溶液自行下滴 放出 快 20S反应结束,放热停止,但随着装置散热,温度会下降,使得三颈瓶内气压开始缓慢减小 催化剂的用量、催化剂颗粒大小或过氧化氢溶液的温度(写溶液的压强不得分)
【解析】 (1)探究有气体参与的反应实验时,要检查装置的气密性,检查A装置气密性的方法是夹住右侧导气管,打开①的两个活塞,向其中加水,若水不滴下(或漏斗下管口有水柱),则气密性良好;(2)反应产生的气体把B中的水压入量筒中,选用C1或C2装置,对该探究实验结论都没有影响;(3)催化剂能改变化学反应速率,反应速率越快催化效果越好从实验数据可知,相同条件下表中催化剂的催化效果由强到弱依次为:活性炭>![]() >
>![]() ;(4)根据题意可知,该探究实验中,需要收集50mL氧气,所以需要测定集50mL氧气的时间;(5)由于过氧化氢在二氧化锰的催化作用下放出热量,气体受热膨胀,体积增大,所以当量筒中收集到50mL水时,双氧水分解出的氧气体积小于50mL; (6)实验中,恒压漏斗的作用是使
;(4)根据题意可知,该探究实验中,需要收集50mL氧气,所以需要测定集50mL氧气的时间;(5)由于过氧化氢在二氧化锰的催化作用下放出热量,气体受热膨胀,体积增大,所以当量筒中收集到50mL水时,双氧水分解出的氧气体积小于50mL; (6)实验中,恒压漏斗的作用是使![]() 溶液自行下滴(使漏斗及三颈瓶成为一个整体);(7)由图1知道:
溶液自行下滴(使漏斗及三颈瓶成为一个整体);(7)由图1知道: ![]() 溶液分解时会放出热量;(8)根据数据可以知道
溶液分解时会放出热量;(8)根据数据可以知道![]() 溶液浓度越高,反应速率越快,以10%
溶液浓度越高,反应速率越快,以10%![]() 溶液为例,20S后三颈瓶内气压由高缓慢降低的原因是:反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;(9)影响
溶液为例,20S后三颈瓶内气压由高缓慢降低的原因是:反应结束,温度下降,气体也因冷却而收缩,使得三颈瓶内气压开始缓慢减小;(9)影响![]() 溶液分解速率的因素,除了催化剂的种类、
溶液分解速率的因素,除了催化剂的种类、![]() 溶液浓度外,还可能与催化剂的用量、催化剂颗粒大小或过氧化氢溶液的温度有关。
溶液浓度外,还可能与催化剂的用量、催化剂颗粒大小或过氧化氢溶液的温度有关。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】空气与人体呼出的气体相比较,下列叙述正确的是( )
①氧气的含量:空气>呼出的气体
②二氧化碳的含量:空气<呼出的气体
③水蒸气的含量:空气>呼出的气体
A. ①② B. ①②③ C. ②③ D. ①③
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】配制20%的氯化钠溶液时,不会引起溶液中氯化钠的质量分数偏小的是( )
A.氯化钠晶体不纯
B.转移已配好的溶液时,有少量液体溅出
C.用量筒取水时仰视读数
D.烧杯用蒸馏水润洗后再配制溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。
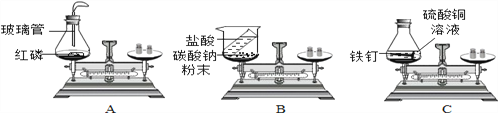
(1)在验证质量守恒定律时,下列A、B、C三个实验设计中,不能达到实验目的的是______(选填序号),理由是_______________。
(2)从微观角度分析,解释反应中,质量守恒定律成立的原因是:_____。
(3)在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | A | B | C | D |
反应前质量/g | 2 | 24.5 | 4 | 8 |
反应后质量/g | 16.9 | 0 | 13.6 | X |
表中X=______,该反应中D物质可能起了_________作用。容器内发生的反应的基本类型是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图,回答有关问题:
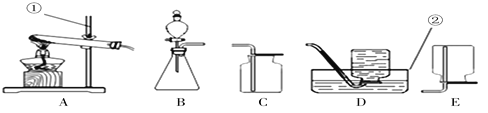
(1)请写出仪器的名称:①_________,②_______。
(2)若选用B装置作为制取氧气的发生装置,其化学方程式是_______________。
(3)用高锰酸钾制取氧气:化学方程式为_________________;如果用A作为发生装置则需________________;如果用D装置收集氧气,当气泡连续均匀冒出时才能收集的原因是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请按要求填空。
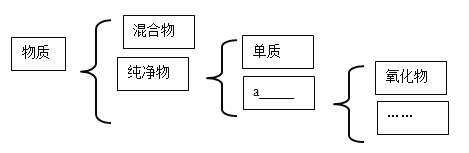
(1)上图中a处应填写____________。
(2)有以下物质①空气、②氧气、③二氧化碳其中属于混合物的是________,(用序号填空,下同)属于单质的是_______,属于氧化物的是____________。
(3)只含有一种元素的物质不可能是____________
A.单质 B.化合物 C.混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]的形式存在。牛奶含钙丰富又易吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。如图是某乳业纯牛奶包装标签的部分文字。请仔细阅读后回答下列问题:

(1)包装标签上脂肪≥3.3g,是指100mL牛奶中,含脂肪的质量至少为3.3g。那么一盒牛奶含钙至少_________g(保留到 0.01g)。
(2)羟基磷酸钙的相对分子质量为_________。
(3)长期缺钙,可能会导致_________病,若人体每天至少需要0.6g钙,且这些钙有90%来自牛奶,则一个人每天至少要喝________盒牛奶。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为Cl9Hl9N7O6。下列有关叶酸的说法中正确的是
A.叶酸的相对分子质量为441 g
B.叶酸中氮元素的质量分数大于氧元素的质量分数
C.叶酸中碳、氢、氮、氧四种元素质量比为19:19:7:6
D.叶酸由19个碳原子、19个氢原子、7个氮原子和6个氧原子构成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com