
分析 (1)根据溶液的质量和溶质的质量分数可以求算溶质的质量.溶液稀释的过程中,溶质的质量保持不变.稀释浓硫酸应该是将浓硫酸沿烧杯壁慢慢倒入水中,且用玻璃棒不停搅拌.
(2)中和反应用pH判断反应进行程度时,当pH=7时,表示酸碱恰好完全反应,根据化学方程式和硫酸的质量求算氢氧化钠的质量,进而结合氢氧化钠溶液的质量分数求算出溶液的质量.
解答 解:
(1)配制100g质量分数为20%的氢氧化钠溶液时,溶质氢氧化钠的质量为100g×20%=20g.
溶液稀释过程中溶质的质量保持不变.
设需要的浓硫酸的质量为x
98%x=100g×9.8%
x=10g.
浓硫酸密度大,且溶解放热,具有很强的腐蚀性,在稀释浓硫酸时,要将浓硫酸慢慢沿烧杯壁倒入水中,且用玻璃棒不停搅拌.
(2)用pH判定酸碱中和反应进行程度时,当pH=7表示两者恰好完全反应.
设反应掉的氢氧化钠的质量为y.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 100g×9.8%
$\frac{80}{98}$=$\frac{x}{100g×9.8%}$
x=8g
则所需要的氢氧化钠的溶液的质量为$\frac{8g}{20%}$=40g
答:消耗氢氧化钠溶液的质量为40g
点评 稀释浓硫酸是初中化学操作中常考的操作点,熟记操作的要求.根据化学方程式计算时,化学方程式要正确,使用数据要准确,过程要完整.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
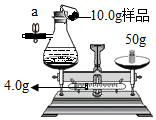 某化学课外活动小组测定长期放置的铁粉中铁单质的百分含量.他们准确称量两份质量各为10.0g的铁粉样品,分别进行如下操作:
某化学课外活动小组测定长期放置的铁粉中铁单质的百分含量.他们准确称量两份质量各为10.0g的铁粉样品,分别进行如下操作:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2O-表示两个氧元素 | B. | N2-表示两个氮原子 | ||
| C. | Ca2+-表示钙元素显+2 | D. | 2H2O-表示2个水分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
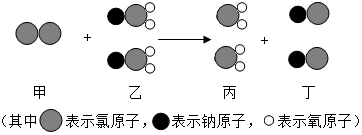
| A. | 该反应属于分解反应 | B. | ClO2中Cl元素的化合价为+2 | ||
| C. | 该反应前后分子的种类和个数不变 | D. | 该反应遵循质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 时间(分钟) | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| 电子天平示数(克) | 110 | 108.2 | 107 | 106.4 | 106.4 | 106.4 | 106.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com