
【题目】现有一瓶含NaCl杂质的Na2CO3样品,某同学设计了一种测定其纯度的方法,装置如图1,其中A容器中盛有样品10.0g,分液漏斗内盛有稀硫酸,B容器内为碱石灰固体。
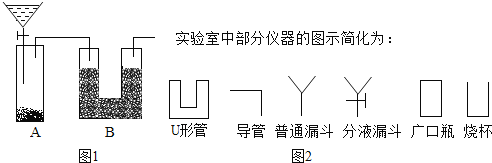
(1)该同学重复操作了三次,每次操作均正确,且装置不漏气,可是结果数据出现了较大偏差(容器内反应均完全,装置内空气的影响忽略不计),请你分析可能的原因______。
(2)通过仔细分析,该同学重新设计了一套实验装置如图3,请回答有关问题:(可供选择的试剂还有Zn片、浓硫酸、NaOH溶液、CaCO3固体、蒸馏水)

①该套装置未画完整,请在你认为需要补充装置的虚框内画出合适的简图,并注明试剂_____。
②A装置的广口瓶中应加入的试剂是______;该装置的作用是______。
③如果实验后测得E装置质量增重3.52g,则该Na2CO3试样的纯度为______。
(3)测定该Na2CO3试样纯度的方法有多种,请你利用不同的反应原理再设计一套方案。要求写出实验操作流程和试样中Na2CO3纯度的表达式。(试剂任选)
操作流程按下列图4所示表述:
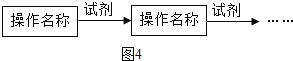
①操作流程为(图5):______。
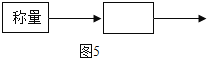
②实验时称量样品的质量为a克,所测物质的质量为b克,该试样中Na2CO3纯度的表达式为:______。
【答案】①A中产生的CO2气体未全部进入B;②CO2中混有的少量水蒸气进入B;③B吸收了空气中的水蒸气、CO2 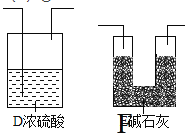 Zn片和蒸馏水 利用A中生成的H2将C中的CO2全部排入E中被碱石灰吸收 84.8%
Zn片和蒸馏水 利用A中生成的H2将C中的CO2全部排入E中被碱石灰吸收 84.8% ![]()
![]()
【解析】
(1)空气中的二氧化碳和水会进入装置B中,与碱石灰反应,碳酸钠与稀硫酸反应生成硫酸钠、二氧化碳和水,二氧化碳会从稀硫酸中携带水蒸气,进入装置B,被碱石灰吸收,也有可能,A中产生的二氧化碳未全部被碱石灰吸收,从而使实验产生误差,所以结果数据出现了较大偏差,可能的原因是:①A中产生的CO2气体未全部进入B;②CO2中混有的少量水蒸气进入B;③B吸收了空气中的水蒸气、CO2;
(2)①浓硫酸有吸水性,所以进入碱石灰之前,需要先用浓硫酸将水蒸气吸收,还要防止空气中的水蒸气和二氧化碳进入碱石灰中,所以需要补充装置的虚框内画出合适的简图为: ;
;
②题中所给的浓硫酸需要稀释,实验室用锌和稀硫酸反应生成氢气,氢气可以将二氧化碳排出,减小实验误差,所以A装置的广口瓶中应加入的试剂是:Zn片和蒸馏水,该装置的作用是:利用A中生成的H2将C中的CO2全部排入E中被碱石灰吸收;
③E装置中增加的质量就是反应生成的二氧化碳的质量。
设参加反应的碳酸钠的质量为x
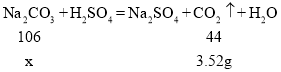
![]() x=8.48g
x=8.48g
所以该Na2CO3试样的纯度为:![]() ;
;
(3)①碳酸钠和氯化钙反应会生成碳酸钙沉淀,通过沉淀的质量计算出碳酸钠的质量,再求出质量分数,所以操作流程是:![]() ;
;
②实验时称量样品的质量为a克,所测物质的质量为b克,所以碳酸钙质量为b,设参加反应的碳酸钠质量为y,所以
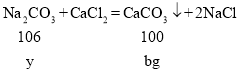
![]() y=
y=![]() g
g
所以碳酸钠的质量分数为: 。
。


科目:初中化学 来源: 题型:
【题目】实验小组用传感器探究稀 NaOH 溶液与稀盐酸反应过程中温度和 pH 的变化。测定结果如图所示,下列说法不正确的是( )
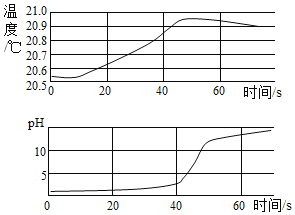
A.反应过程中有热量放出
B.30 s 时,溶液中溶质为 HCl 和 NaCl
C.该实验是将 NaOH 溶液滴入稀盐酸
D.溶液混合,钠离子与氯离子结合生成了氯化钠分子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学小组利用下图装置,多次连续进行氧气的制取和性质的实验。
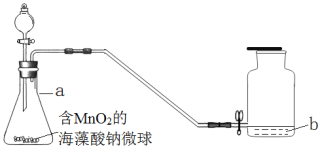
(1)a的仪器名称是______。
(2)该装置制取氧气时,发生反应的化学方程式为______,收集氧气的方法是______。
(3)该实验中,用含MnO2的海藻酸钠微球比直接使用MnO2的优点是______。
(4)进行氧气的性质实验时,实验不同,集气瓶中盛放的物质b不同。
①铁丝燃烧,b为水,其作用是______。
②硫粉燃烧,b为氢氧化钠溶液,其作用是______。
③蜡烛燃烧,b为______,可以验证蜡烛中含有碳元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示的是物质A~G相互间的关系(“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应)A、F都是单质;F是使用最多的金属材料;B是导致温室效应的主要气体;在工业上,C广泛用于玻璃、造纸、纺织和洗涤剂的生产等;D的一种俗名为消石灰;E是一种蓝色溶液。请回答:
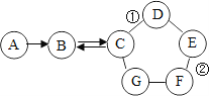
(1)C的化学式______,G可能是______(写名称)。
(2)写出D的一种重要用途______。(合理即可)
(3)写出标号①、②的化学反应方程式①______②______,反应的类型属于______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线。请回答下列问题。
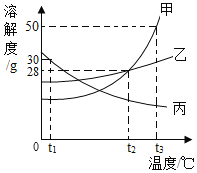
(1)t2℃时甲和______的溶解度相等。
(2)t3℃时50g甲加入50g水中充分溶解后,所得溶液是______(填“饱和”或“不饱和”)溶液,该溶液中溶质与溶剂的质量比为______。
(3)将丙的饱和溶液从t3℃降温到t2℃,一定会发生改变的是______(填字母);
A 溶解度B 溶质的质量C 溶质的质量分数
(4)分别将乙、丙两种物质的饱和溶液各100g从t3℃降到t1℃,降温后乙、丙两种溶液溶质质量分数关系正确的是______(填字母)。
A 乙>丙B 乙=丙C 乙<丙D 不能确定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙是三种单质,其中乙是气体,丙是常见的黑色固体,A、B、C是三种化合物,它们之间有下列转化关系:
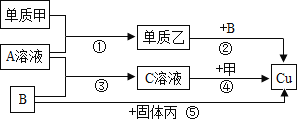
(1)用化学式表示下列物质:B______ 乙______丙______。
(2)写出⑤反应的化学方程式:______;
(3)①至⑤的反应中属于复分解反应的是______(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】比较、分析、归纳是学习化学的有效方法。现有反应如下:
①![]()
②![]()
③![]()
④![]()
(1)通过比较、分析,可以发现上述四个反应有相似之处,均属于四种基本反应类型中的_____反应;
(2)分析反应①和②,可以得到:Zn、Cu、Ag这三种金属的活动性由强到弱的顺序是_____,用相似的思维方法类推到反应③和④中,我们还可以得到Cl2、Br2、I2三种非金属的活泼性强弱是_____,请写出氯气与碘化钾反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我市某地石灰石资源丰富,化学兴趣小组的同学为了测定该石灰石中碳酸钙的质量分数,用托盘天平称取了5份石灰石样品,分别加入各盛有200.0克稀盐酸的烧杯中充分反应(假设杂质不反应),得如下实验数据:
实验编号 | 1 | 2 | 3 | 4 | 5 |
石灰石样品的质量/g | 12.5 | 25.0 | 37.5 | 50.0 | 62.5 |
生成CO2的质量/g | 4.4 | 7.5 | 13.2 | 17.6 | 17.6 |
分析上述实验数据并回答:
(1)实验编号为_______的实验数据有明显错误。
(2)这种石灰石样品中碳酸钙的质量分数为__________。
(3)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从海水中制备纯碱和金属镁的流程如下图所示:
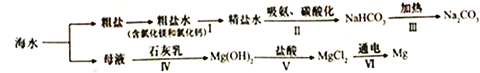
下列说法错误的是
A. 流程I依次向粗盐水中加入过量Ca(OH)2溶液、Na2CO3溶液和适量稀盐酸去除杂质
B. 流程II吸氨是使溶液呈碱性,有利于吸收二氧化碳
C. 上述流程涉及到三种基本反应类型
D. 流程IV、V是通过化学方法富集氯化镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com