
【题目】某白色固体混合物可能含有Na2CO3、 KOH、MgCl2、CaC12中的一种或几种。为了确定该混合物的成份,化学兴趣小组同学进行了如图所示实验:
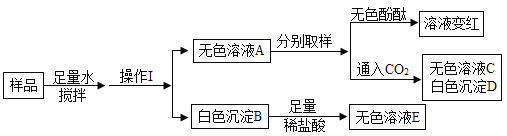
(1)在固体样品中加入足量水搅拌后的操作Ⅰ是__________。
(2)往白色沉淀B中加入足量稀盐酸,沉淀全部溶解且无气泡产生,则反应的化学方程式为_______。
(3)取无色溶液A少量于试管中,通入CO2,得到无色溶液C和白色沉淀D,该步骤发生的化学反应方程式为______。
(4)原白色固体中一定含有的物质是_________。
【答案】过滤 Mg(OH)2+2HCl=MgCl2+2H2O 2KOH+CO2=K2CO3+H2O,K2CO3+CaCl2=CaCO3↓+2KCl KOH、MgCl2、CaCl2
【解析】
根据实验可知:加入足量的水,溶解之后,得到白色沉淀B和无色滤液A,氢氧化钾与氯化镁反应生成氢氧化镁和氯化钾,氯化钙与碳酸钠反应生成碳酸钙和氯化钠,可以推测白色沉淀是两物质反应产生的不溶于水的物质,可能是氢氧化镁或者是碳酸钙;向白色沉淀B中加入足量的稀盐酸,沉淀全部溶解且无气泡产生,氢氧化镁与盐酸反应生成氯化镁和水,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,说明该白色沉淀B为氢氧化镁,不是碳酸钙;将无色溶液A分别取样滴入酚酞,溶液变红,说明溶液呈碱性,可能是氢氧化钾或者是碳酸钠使得酚酞变红,另取样通入二氧化碳,得到白色沉淀D和无色溶液C;可知该白色沉淀D为碳酸钙;因此溶液中存在CaCl2,则无色溶液A中没有Na2CO3;经过以上分析可得:白色固体混合物含有KOH、MgCl2、CaCl2;而没有Na2CO3;代入验证可得推导正确。
(1)在固体样品中加入足量水搅拌后,将固体和液体进行分离,因此操作Ⅰ是过滤;
(2)往白色沉淀B中加入足量稀盐酸,沉淀全部溶解且无气泡产生,说明没有碳酸钙,因此只是氢氧化镁与盐酸的反应,其化学方程式为:Mg(OH)2+2HCl=MgCl2+2H2O;
(3)取无色溶液A少量于试管中,通入CO2,得到无色溶液C和白色沉淀D,该步骤发生反应原理如下:先是二氧化碳与氢氧化钾反应生成碳酸钾和水,再碳酸钾与氯化钙反应生成碳酸钙沉淀,发生的化学反应方程式为:2KOH+CO2=K2CO3+H2O,K2CO3+CaCl2=CaCO3↓+2KCl;
(4)由分析可得:原白色固体中含有的物质是KOH、MgCl2、CaCl2。


科目:初中化学 来源: 题型:
【题目】天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种氧化镍NiO晶体中就存在如下图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代,其结果晶体仍呈电中性,但此化合物中Ni和O的比值却发生了变化。某氧化镍样品组成中个数比Ni∶O=97∶100,
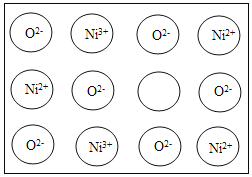
(1)写出该氧化镍样品的化学式_________ 。
(2)试计算晶体中Ni2+与Ni3+的离子个数之比___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列离子能在pH=1的溶液中大量共存形成无色溶液的是( )
A.Na+、![]() 、Cl-、Fe2+B.OH-、K+、
、Cl-、Fe2+B.OH-、K+、![]() 、Ba2+
、Ba2+
C.Mg2+、![]() -、Al3+、
-、Al3+、![]() D.Na+、CO32-、Ca2+、Cl-
D.Na+、CO32-、Ca2+、Cl-
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关“2CO+O2![]() 2CO2”的质量关系,不正确的是( )
2CO2”的质量关系,不正确的是( )
A.若56g CO参加反应,则消耗O2的质量一定是32g
B.若16g O2参加反应,则生成CO2的质量一定是44g
C.若10g CO2生成,则消耗CO和O2的质量总和一定是10g
D.若5g CO和2g O2混合点燃,则CO2生成的质量一定是7g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH)2溶液,烧杯内溶液中的溶质质量变化如图所示(忽略溶液温度的变化),下列分析正确的是( )

A. a点溶液中有两种溶质
B. b点溶液中滴加紫色石蕊溶液,溶液变蓝
C. c点烧杯内液体的pH=7
D. d点溶液中较多的Ba2+、OH﹣、SO42﹣、H+
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向盛有10g49%稀硫酸的烧杯中加入5.6克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是( )
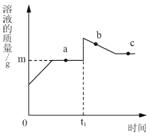
A. 取a点是溶液,加入锌粉,有气体放出
B. b点时,溶液中溶质只有一种
C. c点时,烧杯中固体一定是铜
D. m=12.7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像能正确反映对应变化关系的是
A.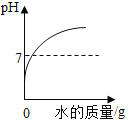 加水稀释氯化钠溶液
加水稀释氯化钠溶液
B.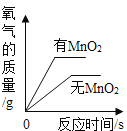 两份等质量的过氧化氢溶液在有、无MnO2的情况下分解产生氧气
两份等质量的过氧化氢溶液在有、无MnO2的情况下分解产生氧气
C.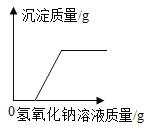 向稀盐酸和硫酸铜的混合溶液中加入氢氧化钠溶液
向稀盐酸和硫酸铜的混合溶液中加入氢氧化钠溶液
D.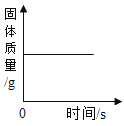 加热碳酸钙
加热碳酸钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据所给内容回答问题:
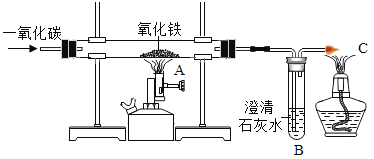
(1)工业上若以赤铁矿为原料来炼铁,其反应原理是____(用化学方程式表示。
(2)在实验室里可利用如图装置制得铁,①实验中可观察到的实验现象:A_____、B_____。C处酒精灯的作用是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式氧化镍(化学式为:NiOOH)可用作镍氢电池的正极材料。工业上以某废液(主要溶质为:硫酸镍,其化学式为:NiSO4,另外还含有一些其他杂质。)为原料生产NiOOH 的步骤如下:
步骤 I:向废液中加入 Na2CO3 溶液生成沉淀,过滤,洗涤,得到固体 NiCO3。
步骤 II:向固体 NiCO3 中加入稀硫酸,固体溶解,得到硫酸镍溶液。
步骤 III:调节硫酸镍溶液的 pH,可将硫酸镍转化为氢氧化镍沉淀(化学式为:Ni(OH)2), 过滤并洗涤沉淀。
步骤 IV:将氢氧化镍沉淀置于空气中加热,生成碱式氧化镍(化学式为:NiOOH)。 请回答以下问题:
(1)NiOOH 中 Ni 的化合价为:_____。
(2)写出向废液中加入 Na2CO3 溶液生成 NiCO3 沉淀的化学方程式_____。
(3)步骤 I 和步骤 II 的作用是:_____。
(4)步骤 IV中生成了碱式氧化镍和水,请写出步骤 IV中发生反应的化学方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com