
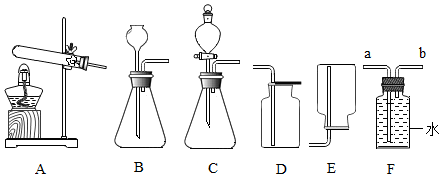
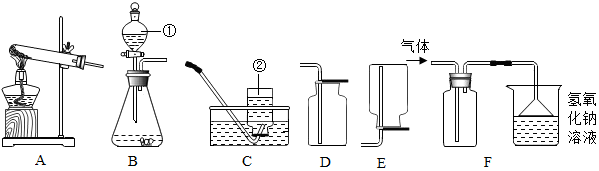
���� ��1�����ݹ��˲����õ�������������
��2�����ݽ���ˮ��Ӳ�ȵķ���������
��3�����ݷ�Ӧ���״̬�ͷ�Ӧ����ѡ����װ�ã������������ܶȺ��ܽ���ѡ���ռ�װ�ã�
��4�����������غ㶨�ɣ��ڻ�ѧ��Ӧǰ��ԭ�ӵ��������Ŀ��û�иı䣮����֪��Ӧ����Cԭ������Ϊ8����������Cԭ������ҲӦ��ΪΪ8����������m=8-2=6��������������ԭ�������ͼ״�����ԭ�������������n=11���ɷ���ʽ�п����ҳ��μӷ�Ӧ������������ˮ�������ȣ���������ˮ������������òμӷ�Ӧ������������
��� �⣺��1��������Ҫ�õ��������д���Ȧ������̨���ձ���©���Ͳ�������
��2�������г�����еķ�������ˮ��Ӳ�ȣ�
��3��ʵ���ҳ���п�������壩��ϡ���ᣨҺ�壩�ڳ����·�Ӧ�Ƶ���������˷���װ��ѡB������ѡ��A�����ڳ����£��ô���ʯ��ʯ��ʯ��ϡ������ȡ�ģ�̼��ƺ����ụ�ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼����ѧ����ʽΪ��CaCO3+2HCl=CaCl2+H2O+CO2����
�������ܶȱ�ˮС��������װ��F���ռ�����������Ӧ�ôӶ̹ܣ�b�ˣ����룬ˮ�ӳ��ܣ�a�ˣ��ų���Ҫ���Ʋ������������ʣ��ɽ�����©����Ϊ��Һ©��������װ��B��Ϊװ��C��
��4��m=8-2=6��
��μӷ�Ӧ�Ķ�����̼����Ϊx
8CH3OH+11O2$\frac{\underline{\;��ȼ\;}}{\;}$6CO2+2CO+16H2O
6��44 16��18
x 14.4g
$\frac{6��44}{x}=\frac{16��18}{14.4g}$
x=13.2g
�𣺣�1��mֵ��6��
��2���μӷ�Ӧ�Ķ�����̼������13.2g��
�ʴ�Ϊ����1������������2����У�
��3����A��CaCO3+2HCl=CaCl2+H2O+CO2������b��C��
��4����6��
��13.2g��
���� ��������Ҫ������ʵ������ȡ���巢��װ�ú��ռ�װ�õ�ѡȡ��Ҫ��ѧ��Ҫ������װ�ú��ռ�װ��ѡ�����������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
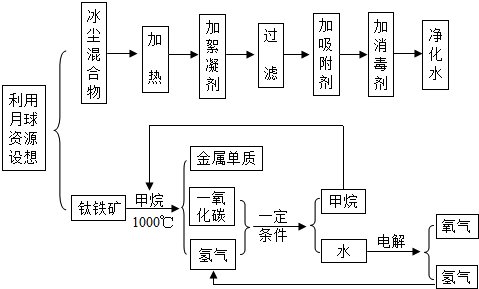
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������̼Ԫ�ء���Ԫ�ء���Ԫ�ع��ɵ� | |
| B�� | �������Է�������Ϊ90 | |
| C�� | ������̼Ԫ������Ԫ�ص�������Ϊ6��1 | |
| D�� | ������̼Ԫ�ص���������Ϊ40% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ˮú���ijɷ���һ����̼������ | |
| B�� | ��Ӧ�к���Ԫ�صĻ����������� | |
| C�� | ��Ӧ�мͱ�������֮��Ϊ4��7 | |
| D�� | ��Ӧǰ��̼Ԫ�صĻ��ϼ�û�з����仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
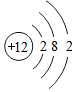 �����ԭ�ӵĵ��Ӳ���Ϊ3�㣬������Ϊ12����Ԫ����ؿ��к������Ԫ�غͿ����к������Ԫ��������Σ�д�����εĻ�ѧʽMg��NO3��2��
�����ԭ�ӵĵ��Ӳ���Ϊ3�㣬������Ϊ12����Ԫ����ؿ��к������Ԫ�غͿ����к������Ԫ��������Σ�д�����εĻ�ѧʽMg��NO3��2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com