
| A. | 在空气中点燃硫,产生明亮的蓝紫色火焰 | |
| B. | 镁条燃烧后生成白色粉末状氧化镁 | |
| C. | 红磷在氧气中燃烧产生大量的白雾 | |
| D. | 木炭在氧气中燃烧发白光 |
科目:初中化学 来源: 题型:选择题
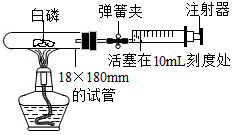 为测定空气中氧气的体积分数,某兴趣小组的同学选用了35mL的试管作反应容器(如图)和量程体积足够大的针筒注射器.将红磷放入试管后,橡皮塞塞紧试管,松开弹簧夹(整套装置的气密性良好).用酒精灯加热红磷,待燃烧结束,冷却到室温,观察现象.可以观察到活塞从原来的10mL刻度处慢慢前移到约( )
为测定空气中氧气的体积分数,某兴趣小组的同学选用了35mL的试管作反应容器(如图)和量程体积足够大的针筒注射器.将红磷放入试管后,橡皮塞塞紧试管,松开弹簧夹(整套装置的气密性良好).用酒精灯加热红磷,待燃烧结束,冷却到室温,观察现象.可以观察到活塞从原来的10mL刻度处慢慢前移到约( )| A. | 1mL刻度处 | B. | 3mL刻度处 | C. | 5mL刻度处 | D. | 8mL刻度处 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子的质量主要集中在原子核上 | |
| B. | 构成物质的微粒只有分子和原子 | |
| C. | 气体易被压缩,说明构成气体的分子在不断运动 | |
| D. | 分子可以分解为原子,原子也可以分解为分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com