
| A. | 一氧化碳和二氧化碳均有可燃性 | |
| B. | 室内放一盆水能防止一氧化碳中毒 | |
| C. | 一氧化碳具有还原性可用于冶炼金属 | |
| D. | 可用氢氧化钠来溶液鉴别某气体是否是二氧化碳 |
分析 A、一氧化碳具有可燃性,通常用作燃料;二氧化碳不能燃烧也不能支持燃烧,常用于灭火;
B、一氧化碳既不能溶解于水也不能与水发生反应,水不能防止一氧化碳的中毒;
C、一氧化碳可以夺取金属氧化物中的氧,使金属氧化物失去氧而变成金属单质;
D、烧碱为氢氧化钠的俗称,能与二氧化碳气体发生反应生成碳酸钠和水,反应时无明显现象.
解答 解:A、一氧化碳具有可燃性,二氧化碳不能燃烧不具有可燃性;故A不正确;
B、一氧化碳不溶解于水、不能与水发生反应,因此室内放一盆水并不能能防止一氧化碳中毒;故B不正确;
C、一氧化碳具有还原性,可与金属氧化物发生氧化-还原反应,而使金属氧化物变成金属单质;故C正确;
D、虽然二氧化碳与氢氧化钠反应生成碳酸钠和水,但反应时无明显现象;因此,不能使用氢氧化钠溶液鉴别二氧化碳气体,故D不正确.
故选C.
点评 对比一氧化碳、二氧化碳两气体的化学性质是本题的考查内容,正确掌握两种物质的化学性质是解答的基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
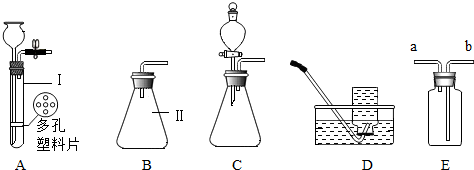
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
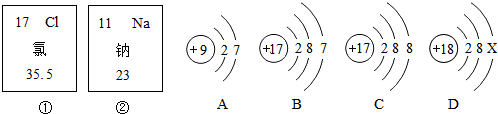
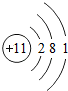 ;
; 查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
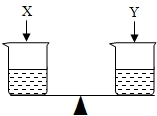 如图在天平两边的烧杯中分别盛有等质量、等质量分数的足量的稀硫酸,然后向左、右两边分别加入X、Y两种等质量的金属,发现天平的指针先偏向右边,最后偏向左边,则X、Y可能是( )
如图在天平两边的烧杯中分别盛有等质量、等质量分数的足量的稀硫酸,然后向左、右两边分别加入X、Y两种等质量的金属,发现天平的指针先偏向右边,最后偏向左边,则X、Y可能是( )| A | B | C | D |
| X:Mg | X:Fe | X:Cu | X:Mg |
| Y:Al | Y:Zn | Y:Fe | Y:Fe |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com