


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
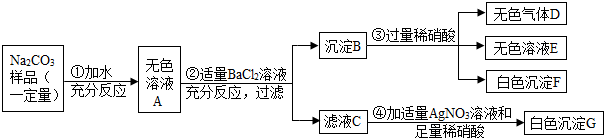
现有某不纯的碳酸钠固体样品,已知其中含有的杂质可能是Na2SO4 、CuSO4 、NaCl、CaCl2中的一种或几种。为确定其杂质的成分,进行如下实验,出现的现象如图所示(设过程中所有发生的反应都恰好完全进行)。
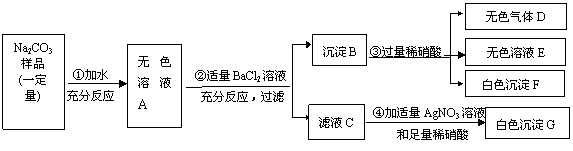 |
请你根据实验过程和发生的现象做出分析判断,并填写以下空白:
(1)把气体D通入紫色石蕊试液中,观察到的现象是 。
白色沉淀G的化学式是 。
(2)碳酸钠固体样品中一定含有的杂质是(写化学式) 。
(3)碳酸钠固体样品中一定不含有的杂质是(写化学式) 。
(4)请写出过程②中发生反应的一个化学方程式 。
(5)碳酸钠固体样品中还不能确定的物质是(写化学式) ,要确定它是否存在,可用溶液A再实验。请简述你的设计方案(说明实验操作步骤、发生的现象及结论):
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com