

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:初中化学 来源: 题型:选择题
| A. | 一切物质都是由分子构成的 | |
| B. | 分子是化学变化中的最小粒子 | |
| C. | 分子是不能再分的粒子 | |
| D. | 分子是保持物质化学性质的最小粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气是一种最轻的气体 | |
| B. | 氢气燃烧产热大,产物无污染,故可做汽车的燃料电池 | |
| C. | 空气中只要混入了氢气,在点燃时一定会发生爆炸,因此点燃氢气前,一定要验纯 | |
| D. | 氢气燃烧时,产生淡蓝色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①④⑤ | C. | ②④ | D. | ②⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
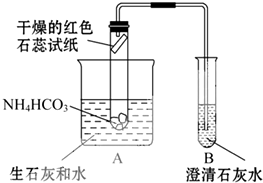
| 实验步骤 | 实验现象 | 反应的化学方程式 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 下列是探究空气中氧气所占体积的实验
下列是探究空气中氧气所占体积的实验查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 金属的使用范围特别广.现探究金属与酸溶液反应快慢与哪些因素有关.陈璐、魏松明、韩俊洋、徐庚辰4位同学分别做了下列实验:
金属的使用范围特别广.现探究金属与酸溶液反应快慢与哪些因素有关.陈璐、魏松明、韩俊洋、徐庚辰4位同学分别做了下列实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com