
 CaO+CO2↑)
CaO+CO2↑) CaO+CO2↑
CaO+CO2↑ x=44t
x=44t ×100%=40t
×100%=40t CaO+CO2↑
CaO+CO2↑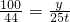 y=56.8t
y=56.8t

科目:初中化学 来源:2011-2012学年山东省九年级12月学业测评化学试卷 题型:选择题
下列化学方程式书写正确的是
A.工业上通过高温煅烧石灰石来生产生石灰:CaCO3 ==== CaO+CO2↑
B.工业上用稀盐酸除铁锈 Fe2O3+ 6HCl==== 2FeCl2 + 3H2O
C.用澄清石灰水检验二氧化碳气体Ca(OH)2+CO2====CaCO3↓+H2O
D.用熟石灰处理硫酸厂中的废水Ca(OH)2+H2SO4====CaSO4 +H2O
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.工业上通过高温煅烧石灰石来生产生石灰:CaCO3═CaO+CO2↑ |
| B.工业上用稀盐酸除铁锈 Fe2O3+6HCl═2FeCl2+3H2O |
| C.用澄清石灰水检验二氧化碳气体Ca(OH)2+CO2═CaCO3↓+H2O |
| D.用熟石灰处理硫酸厂中的废水Ca(OH)2+H2SO4═CaSO4+H2O |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年山东省济宁市邹城市田黄中学九年级(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源: 题型:
| A.工业上通过高温煅烧石灰石来生产生石灰:CaCO3 ="===" CaO+CO2↑ |
| B.工业上用稀盐酸除铁锈 Fe2O3+ 6HCl="===" 2FeCl2 + 3H2O |
| C.用澄清石灰水检验二氧化碳气体Ca(OH)2+CO2====CaCO3↓+H2O |
| D.用熟石灰处理硫酸厂中的废水Ca(OH)2+H2SO4====CaSO4 +H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com