
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示。请回答: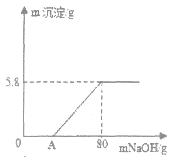
(1)OA段无沉淀产生,请写出反应的化学方程式
(2)加入镁粉的质量为 g;
(3)求产生氢气的质量是多少g?(写出计算过程,保留小数点后一位)。
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:初中化学 来源: 题型:探究题
(10分)二十一世纪是海洋开发与利用的世纪,某市规划确立了“蓝色经济”发展战略,海洋化学资源的综合利用将是重点发展领域之一。以下是某研究性学习小组在探究海水综合利用中遇到的问题,请你参与探究:
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳。
乙:高温加热蒸发海水后,加入石灰乳。
丙:向晒盐后的卤水中,加入石灰乳。
通过分析比较,你认为___________的设想最为经济合理(选填“甲”、“乙”或“丙”)。
问题二、粗盐提纯过程中如何除去可溶性杂质?
【查阅资料】
粗盐中含有硫酸钠、氯化钙等可溶性杂质。
【设计实验】
提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是_____①________;再加过量的____②______,除尽杂质阳离子;滤去沉淀,向滤液中加入__③_____,将溶液的pH调为7,即得到精盐水。
问题三、海水“制碱” 的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行
了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中只含有氢氧化钠;
丙的猜想:样品中含有碳酸钠和氢氧化钠。
他们做出上述三种猜想的科学依据是________________________________。
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全 溶解,再加入________________ | _____________________ | 乙的猜想 不成立 |
| 2 | 取步骤1反应后的溶液于试管中 ___________________________ | 无明显现象 | 只有甲的 猜想成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
一同学用某种粗盐进行提纯实验,步骤见下图。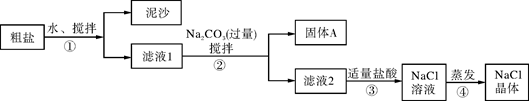
请回答:
(1)步骤①和②的操作名称是 。
(2)步骤③判断加入盐酸“适量”的方法是 ;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止 ,当蒸发皿中有较多量固体出现时,应 ,用余热使水分蒸干。
(3)猜想和验证:
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入 ,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水, | | 猜想Ⅲ成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
牙膏中常用碳酸钙、二氧化硅等物质作为摩擦剂.某同学对牙膏中摩擦剂碳酸钙的含量进行探究.
【实验原理】测定C装置中生成的BaCO3沉淀的质量,通过计算确定牙膏中CaCO3的质量分数.
【查阅资料】CO2+Ba(OH)2=BaCO3↓+H2O,牙膏中其他成分遇到盐酸时无气体产生.
【实验装置】
根据探究过程回答下列问题:
(1)装置B中发生反应的化学方程式 ;
(2)实验过程中需持续缓缓通入空气,其作用有:①搅拌B、C 中的反应物,使其充分反应;② ;
(3)从C中过滤出BaCO3沉淀所需的玻璃仪器有烧杯、 和玻璃棒;
(4)实验中准确称取三份牙膏样品,每份4.0g,进行三次测定,测得生成BaCO3的平均质量为1.97g.则样品中CaCO3的质量分数为 ;
(5)若没有A装置,直接通入空气,则测得CaCO3的质量分数 (填“偏大”、“偏小”或“不变”).
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某化学实验小组欲探究盐酸、氢氧化钙的化学性质,取8支试管分别用A﹣H编号后,做如下实验.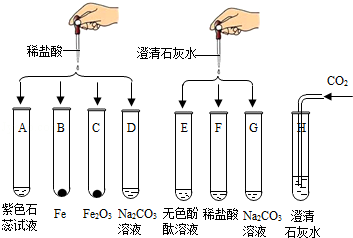
(1)实验中观察到有气泡出现的试管是 ,有沉淀生成的试管是 .
(2)实验后某试管中为红色溶液,当向其中加入过量的NaOH溶液后,溶液变为蓝色.由此推断,该试管中最初盛有的物质是 .
(3)写出实验中无明显现象产生的试管中发生的化学方程式 .
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
(10分)过氧化钙(CaO2)是一种对环境友好的多功能无机化合物,通常有两种制备方法。已知:温度过高过氧化钙会分解生成氧化物和氧气。
方法1:由Ca(OH)2为原料最终制得,其制备流程如下:
方法2:由鸡蛋壳(含CaCO3高达90%)为原料最终反应制得,其制备流程如下: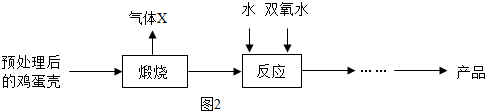
(1)方法1中搅拌的目的是 。请将搅拌过程中发生反应的化学方程式补充完整:
CaCl2 + H2O2 + 2NH3·H2O + 6 = CaO2·8H2O↓+ 2NH4Cl。制备过程中除水外可循环使用的物质是 (填化学式);
(2)方法2中气体X是 ,实验室常用 溶液来吸收。煅烧后的反应时化合反应,也能生成CaO2·8H2O,反应的化学方程式为 。该反应需控制温度在0 ~ 2℃,可将反应器放置在 中,获得CaO2产品中主要含有的固体杂质是 (填化学式);
(3)这两种制法均要求在低温下进行(除煅烧外),温度过高除了防止氨水挥发外,还能 ;
(4)“绿色化学”一般是指反应物的原子全部转化为期望的最终产物,则上述两种方法中生成CaO2·8H2O的反应符合“绿色化学”的是 (填“方法1”或“方法2”)。
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
有一包固体粉末,可能含有氧化钙、氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答: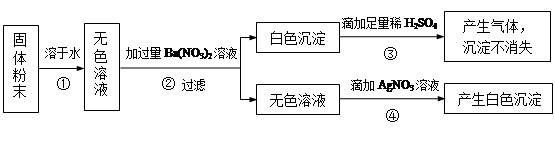
(1)写出步骤④中产生白色沉淀的化学方程式______。
(2)根据实验中的现象,能否确定原固体粉末的组成?若能,请写出各成分的化学式;若不能,在原实验步骤的基础上,对上述方案中的试剂作一改进,并描述相应的实验现象及结论,以确定固体粉末的组成。____________。
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
课外探究小组对实验教师提供的一包白色固体(可能是NaCl、Na2SO4、Na2CO3和NaNO3的一种或几种)进行了下面的实验,且每步实验中均加入足量的试剂,至充分反应。实验过程、现象见下图:
请分析实验过程并完成以下问题:
(1)实验中不能用稀盐酸代替稀硝酸的原因是 ;
(2)滴加Ba(NO3)2的目的是 ;
(3)通过计算推断:原白色固体的成分为 。(简单写出必要的计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:信息分析题
某固体可能由Na2SO4,NaCl,Na2CO3,KNO3中的一种或几种组成,现进行如下实验:
试回答:
⑴.白色沉淀A的化学式为________________;
⑵.原固体中一定含有_______________________,一定不含有_______________________,
可能含有____________________;
⑶.为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:(请补充完整)
取少量固体溶于水,____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com