
分析 ①根据化学方程式的书写方法分析解答.
(1)pH为13的水溶液显碱性,水溶液中含有大量的OH-;根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可;
(2)根据离子方程式的书写方法进行分析.
(3)根据复分解反应的实质进行分析.
解答 解:①K2SO4与BaCl2反应的化学方程式:K2SO4+BaCl2=BaSO4↓+2KCl;故填:K2SO4+BaCl2=BaSO4↓+2KCl.
(1)pH为13的水溶液显碱性,水溶液中含有大量的OH-;
A、Mg2+、OH-两种离子能结合成氢氧化镁沉淀,不能大量共存,故选项错误.
B、四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确.
C、Cu2+、OH-两种离子能结合成氢氧化铜沉淀,不能大量共存,故选项错误.
D、四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确.
故选BD;
(2)稀硫酸和碳酸钠溶液所发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑;故填:CO32-+2H+=H2O+CO2↑;
(3)与离子方程式Ag++Cl-═AgCl↓相对应的化学方程式为HCl+AgNO3═AgCl↓+HNO3,故填:HCl+AgNO3═AgCl↓+HNO3
点评 本题考查的是复分解反应的条件和复分解反应的实质,完成此题,可以依据已有的知识进行.


 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:解答题
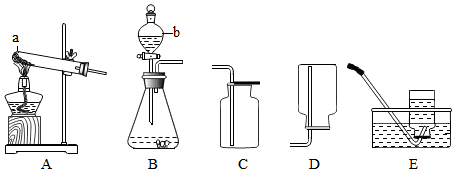
| 实验序号 | ① | ② | ③ | ④ |
| ag大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| bg盐酸 | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤时,漏斗里的液体液面要低于滤纸的边缘 | |
| B. | 溶解和过滤操作中,玻璃棒的作用相同 | |
| C. | 蒸发时,将蒸发皿内液体蒸干后停止加热 | |
| D. | 溶解时,在量筒中边加粗盐边搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用硫酸除铁锈:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 复分解反应 | |
| B. | 工业高炉炼铁:2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ 置换反应 | |
| C. | 除去氢氧化钠溶液中的硫酸钠杂质:Na2SO4+BaCl2=BaSO4↓+2NaCl 复分解反应 | |
| D. | 沼气燃烧提供热量:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2↑ 化合反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com