
【题目】请分别写出下列各组实验的有关现象. 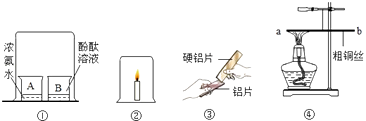
【答案】解:①浓氨水具有挥发性,挥发出的氨气溶于B烧杯使溶液显碱性,酚酞遇碱性溶液变红,因此B烧杯内液体变为红色; ②蜡烛燃烧消耗氧气,因此蜡烛逐渐熄灭;
③硬铝的硬度比铝片大,因此铝片上有划痕;
④在加热条件下,铜与氧气反应生成氧化铜,质量增加,因此冷却后粗铜丝b端略上升.
答:①B烧杯内液体变红色②蜡烛逐渐熄灭;③铝片上有划痕;④冷却后粗铜丝b端略上升.
【解析】根据常见实验的现象进行分析解答即可.
【考点精析】通过灵活运用合金的定义与性能和质量守恒定律及其应用,掌握合金:由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质.一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好;①质量守恒定律只适用于化学变化,不适用于物理变化;②不参加反应的物质质量及不是生成物的物质质量不能计入“总和”中;③要考虑空气中的物质是否参加反应或物质(如气体)有无遗漏即可以解答此题.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图所示是气体制取与性质验证的组合实验.打开A中分液漏斗活塞后,A,B,C,D,E中均可观察到明显现象. 
(1)A中发生反应的化学方程式为 .
(2)B中的现象是 .
(3)E中的现象 , 产生此现象的原因是(用化学方程式解释).
(4)F装置收集的气体是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某化学反应的微观示意图.下列说法错误的是( ) 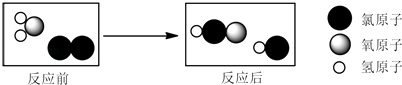
A.该反应前后元素种类不变
B.反应前后氯元素共显示三种化合价
C.参加反应的两物质的质量比为 1:1
D.反应后的物质溶于水形成的溶液的 pH<7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化工厂的废液中含有硝酸银、硝酸亚铁和硝酸锌.某同学取适量的上述废液样品,将一定质量的镁粉加入样品中,充分反应后过滤,得到滤液和滤渣.请回答下列问题: 
(1)若得到的滤液为浅绿色,则滤液中一定含有哪些溶质?(写化学式)
(2)若得到的滤液为无色,则滤渣中一定含有什么物质?(写化学式)
(3)请写出该实验过程中一定发生的反应的化学方程式.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有人认为“氮肥壮叶,磷肥壮果,钾肥壮茎”,小王家的柑橘树结的果实偏小,小王应向柑橘树施加下列化肥中的( )
A. 硫酸钾 B. 硫酸铵 C. 碳酸氢铵 D. 过磷酸钙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】气体的制法、性质和用途等是中学化学研究的重要内容.
(1)请从图1中选择适当的仪器组装实验装置. 
①实验室制取二氧化碳,应选择上面仪器中的(填字母代号).
②若用高锰酸钾制取氧气,还需要补充的一种仪器是(填名称),反应的化学方程式为
(2)小明同学采用如图2装置进行趣味实验. ①若 A 中是碳酸氢钠和稀盐酸,B 中是紫色石蕊溶液,
A 中反应的化学方程式为 , B 中可观察到的现象为 .
②若换一组药品,用所得干燥气体充气球,气球在空中上升,则 A,B 中应分别盛放、(写一组即可).
(3)某同学用过氧化氢溶液和二氧化锰制取氧气,该同学取 50g 过氧化氢溶液和 1g 二氧化锰混合,完全反应后,称量剩余物质的质量为 49.4g.试计算过氧化氢溶液中溶质的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在《联合国气候变化框架公约》大会上通过的《京都协议》中明确规定:发达国家要限制二氧化碳等温室气体的排放量。科学家采取“组合转化”技术,将二氧化碳在一定条件下转化为重要的化工原料乙烯(C2H4),其化学方程式为:2CO2+6H2=C2H4+4H2O。
若用36 g氢气转化二氧化碳,则能处理标准状况下的二氧化碳气体多少升?同时又能生成多少克化工原料乙烯?(已知:标准状况下,二氧化碳的密度为1.977 g/L)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是一门研究物质的科学,我们一般从物质的存在、性质、制备、用途等方面研究一种物质或一类物质,以金属为例,请你参与其中回答相关问题.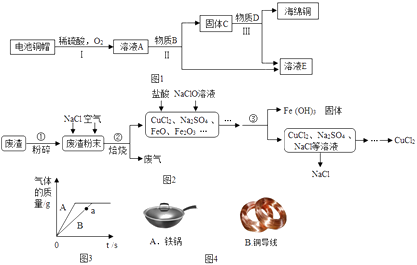
(1)如图4金属制品中,利用金属的物理性质是(至少两条).
(2)亮亮做家务时接触到一袋脱氧剂(主要成分是还原铁粉),拆开后看到还原铁粉已生锈,铁生锈的原因是 , 废旧钢铁表面的铁锈可用盐酸除去,其原理是(写化学方程式).
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图1(反应条件略去).已知:2Cu+2H2SO4+O2 ![]() 2CuSO4+2H2O
2CuSO4+2H2O
①A﹣E中含铜、锌两种元素的物质有(填字母序号).
②我国早在西汉时期,就有“曾青得铁则化为铜”的记述,该反应的化学方程式可表示为
(4)炼铁产生的废渣中含有大量CuS,及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如图2所示:
①在Ⅱ中CuS、NaCl和O2在高温条件下反应生成了CuCl2和Na2SO4 , 其反应的化学方程式是 .
②Ⅲ的操作名称是 , 分离混合物的一般思路,首先分析混合物的组成成分,寻找各成分的差异,然后利用其差异选择合适方法进行分离,该方法就是利用混合物中不同成分差异进行分离的方法.
(5)等质量的A、B两种金属分别与等质量溶质质量分数的稀盐酸充分反应,反应产生气体的质量与反应时间的关系如图3所示,若A、B为Mg、Zn中的一种,则A是 , 反应结束后只有一种金属剩余,则剩余金属为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com