
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以2个水分子可表示为2H2O;
(2)氯酸钾是由显+1价的钾元素和显-1价的氯酸根组成,根据化合价原则,其化学式为:KClO3;
(3)组成氯化钠的微粒是钠离子和氯离子,离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故钠离子和氯离子可表示为:Na+、Cl-;
(4)水在化学反应中的最小粒子是氢原子和氧原子,其符号分别为:H、O;
故答案为:(1)2H2O;(2)KClO3;(3)Na+、Cl-;(4)H、O;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.


科目:初中化学 来源: 题型:填空题
| 实验操作 | 实验现象 |
| ①中加入少量明矾,搅拌静置 | 天然水变澄清 |
| ②中加入少量硫酸铝,搅拌静置 | 天然水变澄清 |
| ③中加入少量硫酸钾,搅拌静置 | 天然水仍浑浊 |
| ④中加入少量氯化铝,搅拌静置 | 天然水变澄清 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
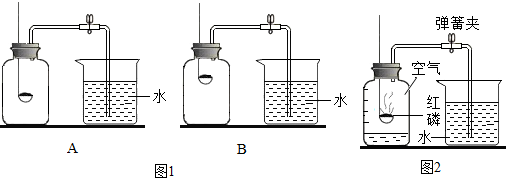
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积/mL | 20 | 21 | 19 | 20 | 22 | 19 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “墙内开花,墙外香”--分子在不断地运动 | |
| B. | 湿衣服晾在有太阳的地方比晾在没有太阳的地方容易干--温度高分子的运动速度加快 | |
| C. | 热胀冷缩--分子的大小随着温度的改变而改变 | |
| D. | 水电解生成氢气和氧气--在化学变化中,分子分解成原子,原子又构成新的分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,该方法是以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:
1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,该方法是以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
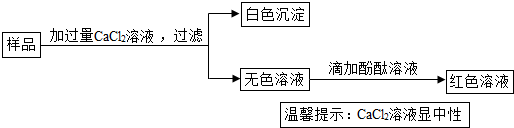
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com