
 现有A~D四种常见物质.它们在一定条件下有如图转化关系:
现有A~D四种常见物质.它们在一定条件下有如图转化关系:分析 根据A~D四种常见物质,若A是常用于改良酸性土壤的碱,D是常用的气体肥料,所以A是氢氧化钙,D是二氧化碳,氢氧化钙会转化成C,C和二氧化碳可以相互转化,所以C是碳酸钙,B是氧化钙;A、B、C、D是不同类别的四种物质,若A是一种黑色固体,C是一种蓝色溶液,所以A是氧化铜,C是氯化铜,B是铜,氯化铜和D可以相互转化,所以D是氢氧化铜,然后将推出的物质进行验证即可.
解答 解:A~D四种常见物质,
(1)若A是常用于改良酸性土壤的碱,D是常用的气体肥料,所以A是氢氧化钙,D是二氧化碳,氢氧化钙会转化成C,C和二氧化碳可以相互转化,所以C是碳酸钙,B是氧化钙,经过验证,推导正确,所以A是Ca(OH)2,C转化为D的反应是碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(2)A、B、C、D是不同类别的四种物质,若A是一种黑色固体,C是一种蓝色溶液,所以A是氧化铜,C是氯化铜,B是铜,氯化铜和D可以相互转化,所以D是氢氧化铜,经过验证,推导正确,所以A转化为C的反应是氧化铜和盐酸反应生成氯化铜和水,化学方程式为:CuO+2HCl=CuCl2+H2O,D转化为C的反应是氢氧化铜和盐酸反应生成氯化铜和水,化学方程式为为:Cu(OH)2+2HCl=CuCl2+2H2O.
故答案为:(1)Ca(OH)2,CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(2)CuO+2HCl=CuCl2+H2O,Cu(OH)2+2HCl=CuCl2+2H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:多选题
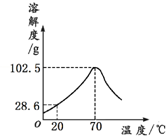 甲物质的溶液可用作化肥、电镀液等.甲的溶解度曲线如图所示,下列说法正确的是( )
甲物质的溶液可用作化肥、电镀液等.甲的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度随温度的升高而增大 | |
| B. | 20℃时,100 g甲的饱和溶液中溶质质量为28.6 g | |
| C. | 将70℃甲的饱和溶液升高温度,有晶体析出 | |
| D. | 70℃时,甲的饱和溶液的溶质质量质量分数为50.6% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 掌握好分类规律和加强对实验的理解是学好初中化学的重要途径.
掌握好分类规律和加强对实验的理解是学好初中化学的重要途径.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
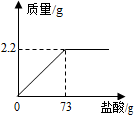 现有家庭食用碱样品8g(主要成分Na2CO3和NaCl),向其中加入100克某未知浓度的盐酸,生成气体的质量与加入盐酸的质量关系如图.请计算:
现有家庭食用碱样品8g(主要成分Na2CO3和NaCl),向其中加入100克某未知浓度的盐酸,生成气体的质量与加入盐酸的质量关系如图.请计算:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com