考点:食品干燥剂、保鲜剂和真空包装的成分探究,常见气体的检验与除杂方法,化学式的书写及意义,元素的质量分数计算,化合物中某元素的质量计算,燃烧、爆炸、缓慢氧化与自燃
专题:科学探究
分析:(1)根据食品易变质的条件,氧气能使食品发生缓慢氧化而变质,据此进行分析解答.
(2)检验某铁粉是否还有效,根据金属的化学性质进行分析解答.
(3)食物腐败变质是由于微生物的生长和大量繁殖而引起的.根据食物腐败变质的原因,食品保存就要尽量的杀死或抑制微生物的生长和大量繁殖.将食物放在冰箱中就是利用冰箱内的低温环境抑制了微生物的生长和繁殖,来达到较长时间保存的目的.因此若一次性购买了较多的这种牛奶,可以用低温方法储存,理由是低温可抑制细菌生长繁殖.
(4)①根据二氧化碳的性质可以选择澄清石灰水来进行验证;
②二氧化碳可以使澄清石灰水变浑浊,所以可以据此完成该题的解答;
③既然是食品首先要保证是无毒,同时要保证食品的质量,可以据此作答.
(5)①根据丙酸钠化学式为C
3H
5O
2Na,利用各元素的相对原子质量与分子中原子个数的乘积之比,计算丙酸钠中C、H、O、元素的质量比;
②由苯甲酸钠的化学式来判断苯甲酸钠的元素组成;
③由苯甲酸钠的化学式来判断每个苯甲酸钠分子中含有多少个原子;
④利用
| 碳的相对原子质量×苯甲酸钠分子中碳元素的原子个数 |
| 苯甲酸钠的相对分子质量 |
×100%来计算苯甲酸钠中碳元素的质量分数;
⑤依据物质中某元素的质量分数的计算方法来计算72g苯甲酸钠含钠元素质量与多少克氯化钠中所含钠元素质量相当;
⑥要计算50Kg面粉最多添加多少苯甲酸钠,须按苯甲酸钠在食品中的最大允许使用量即1g/kg来计算.
解答:解:
(1)空气中的氧气具有氧化性,而微生物繁殖需要氧气,所以在没有氧气的情况下,微生物难以繁殖;同时没有氧气,可以防止食物发生缓慢氧化而变质;故填:氧;氧化;
(2)铁粉用作防腐剂,主要是利用铁粉生锈时消耗氧气,而使食物与氧气隔离.故填:铁粉吸收氧气和水分,使食品不被氧化并保持干燥
(3)将食物放在冰箱中就是利用冰箱内的低温环境抑制了微生物的生长和繁殖,来达到较长时间保存的目的.故填:低温可抑制细菌生长繁殖,延长食品保质期
(4))【猜想与验证】根据二氧化碳的性质,可以用澄清石灰水来检验小明的猜想,具体的步骤为:用注射器抽取包装袋内的气体,然后通入适量的澄清石灰水中,澄清石灰水会变浑浊;其中发生反应的表达式:Ca(OH)
2+CO
2═CaCO
3↓+H
2O;包装袋的气体必须是无毒的、比较稳定的,例如氮气、二氧化碳等,充入的气体还可能是:氮气;
【反思】因为是对食品充气包装,所有对所充气体须要求:①气体无毒;②化学性质不活泼;③不能与食品反应;
(5)
(5)①根据丙酸钠化学式为C
3H
5O
2Na,利用各元素的相对原子质量与分子中原子个数的乘积之比,计算丙酸钠中C、H、O、元素的质量比:12×3:1×5:16×2=36:5:32;即丙酸钠中C、H、O元素的质量比是:36:5:32;
②苯甲酸钠的化学式是C
7H
5NaO
2,所以苯甲酸钠是有碳、氢、钠、氧四种元素组成的;
③苯甲酸钠的化学式是C
7H
5NaO
2,每个苯甲酸钠分子中含有7个碳原子、5个氢原子、1个钠原子、2个氧原子,所以每个苯甲酸钠化学式中含有15个原子;
④利用
| 碳的相对原子质量×苯甲酸钠分子中碳元素的原子个数 |
| 苯甲酸钠的相对分子质量 |
×100%来计算苯甲酸钠中碳元素的质量分数:
×100%=
×100%=57.5%(精确到0.1%);
⑤设72g苯甲酸钠含钠元素质量与x克氯化钠中所含钠元素质量相当,依据物质中某元素的质量分数的计算方法,72g×
×100%=x×
×100%,所以x=29.4g,即72g苯甲酸钠含钠元素质量与29.4克氯化钠中所含钠元素质量相当;
⑥苯甲酸钠在食品中的使用量为0.2-1g/kg.现有50Kg面粉要加工成面包,最多添加苯甲酸钠的质量:50kg×1g/kg=50g.
本题答案为:
(1)氧;氧化;
(2)铁粉吸收氧气和水分,使食品不被氧化并保持干燥;
(3)低温可抑制细菌生长繁殖,延长食品保质期;
(4)【猜想与验证】用注射器抽取包装袋内的气体通入澄清石灰水中,澄清石灰水变浑浊;Ca(OH)
2+CO
2═CaCO
3↓+H
2O;氮气;
【反思】气体无毒;化学性质不活泼;不能与食品反应;(5)①36:5:32;
②C、H、Na、O;③15;④57.5%;⑤29.4克;⑥50g;
点评:本题考查了食品中常见的充入气体二氧化碳和氮气,并涉及到气体的检验,应该明确二氧化碳化学性质及其检验方法.还考察了关于化学式的计算,知识熟练是关键.



 优生乐园系列答案
优生乐园系列答案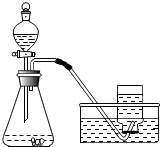 实验室制取氧气的装置如图所示,下列有关叙述合理的是( )
实验室制取氧气的装置如图所示,下列有关叙述合理的是( )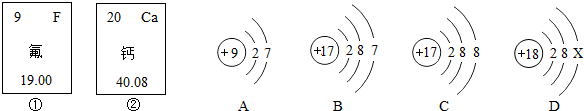
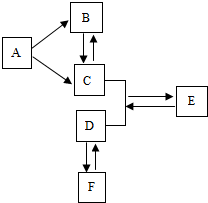 A~F表示几种初中化学常见的物质,它们之间的关系如图所示(图中“→”表示两端的物质间能发生化学反应,“---”表示物质间存在转化关系).C是一种最常用的溶剂;F是氧化物,其中两种元素质量之比为3:4.
A~F表示几种初中化学常见的物质,它们之间的关系如图所示(图中“→”表示两端的物质间能发生化学反应,“---”表示物质间存在转化关系).C是一种最常用的溶剂;F是氧化物,其中两种元素质量之比为3:4.